Hvad er et polært molekyle, der har en let negativ ladning nær elementet?
* polært molekyle: Et molekyle, hvor elektronerne ikke deles lige mellem atomerne. Dette skaber en adskillelse af ladning, med den ene ende af molekylet lidt positivt og den anden lidt negativ.
* delvis negativ ladning: Dette forekommer på atomet, der tiltrækker elektroner stærkere i en kovalent binding. Dette atom vil have en lidt højere elektrondensitet, hvilket gør det lidt negativt.
Eksempel:
* vand (H₂O): Oxygen er mere elektronegativ end brint. Dette betyder, at det trækker de delte elektroner i de kovalente bindinger tættere på sig selv. Oxygenatomet udvikler en delvis negativ ladning (Δ-), mens brintatomerne udvikler delvis positive ladninger (Δ+).
Sådan identificeres:
* Elektronegativitet: Se efter et molekyle med atomer, der har en signifikant forskel i elektronegativitet. Det mere elektronegative atom har den delvise negative ladning.
* molekylær geometri: Molekylets form spiller også en rolle. Et molekyle med en bøjet eller asymmetrisk form er mere tilbøjelig til at være polær.
Eksempler på polære molekyler med delvis negative ladninger:
* ammoniak (NH₃): Nitrogen har en delvis negativ ladning.
* hydrogenfluorid (HF): Fluor har en delvis negativ ladning.
* ethanol (C₂H₅OH): Oxygen har en delvis negativ ladning.
Fortæl mig, hvis du vil have flere eksempler eller have specifikke elementer i tankerne!
Sidste artikelDen funktionsgruppe indeholdt i den sammensatte CH3 -CH2 -O -CH3 er en?
Næste artikelReagerer med ilt for at producere rust?
 Varme artikler
Varme artikler
-
 Ny klasse af materialer kunne bruges til at lave batterier, der oplades hurtigereKredit:CC0 Public Domain Forskere har identificeret en gruppe materialer, der kunne bruges til at lave batterier med endnu højere effekt. Forskerne, fra University of Cambridge, brugte materialer
Ny klasse af materialer kunne bruges til at lave batterier, der oplades hurtigereKredit:CC0 Public Domain Forskere har identificeret en gruppe materialer, der kunne bruges til at lave batterier med endnu højere effekt. Forskerne, fra University of Cambridge, brugte materialer -
 Skaber grønt protein fra luftenKredit:CC0 Public Domain Stigende miljømæssige udfordringer har fået forskere til at genoverveje, hvordan protein kan produceres. Traditionelle processer kræver meget plads til lands eller til van
Skaber grønt protein fra luftenKredit:CC0 Public Domain Stigende miljømæssige udfordringer har fået forskere til at genoverveje, hvordan protein kan produceres. Traditionelle processer kræver meget plads til lands eller til van -
 Opdagelsen af livsforlængende vej hos orme viser en ny måde at studere aldring påCaenorhabditis elegans. Kredit:Wikipedia Et enzymblokerende molekyle kan forlænge levetiden for Caenorhabditis elegans rundorme med så meget som 45 procent, hovedsagelig ved at modulere en cannabi
Opdagelsen af livsforlængende vej hos orme viser en ny måde at studere aldring påCaenorhabditis elegans. Kredit:Wikipedia Et enzymblokerende molekyle kan forlænge levetiden for Caenorhabditis elegans rundorme med så meget som 45 procent, hovedsagelig ved at modulere en cannabi -
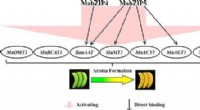 Appellerende fund tyder på, hvorfor køling dæmper bananaromaerKredit:American Chemical Society Bananer er en af verdens mest populære frugter. Men hvordan de opbevares, før de når dagligvarehylderne, kan påvirke deres smag og lugt negativt. Nu i en undersø
Appellerende fund tyder på, hvorfor køling dæmper bananaromaerKredit:American Chemical Society Bananer er en af verdens mest populære frugter. Men hvordan de opbevares, før de når dagligvarehylderne, kan påvirke deres smag og lugt negativt. Nu i en undersø
- Den mest afsidesliggende ø skaber en massiv havbeskyttelseszone
- Her er hvad politiet ved om digitale beviser
- Nedbrydningen af 10 g ammoniak producerer brint- og nitrogengasser frigiver 6300 cal energi. Hvor …
- Hvad er der i et navn? Nogle gange klimaet
- Hvordan virker en oliefremstilling?
- Dette område af jorden består hovedsageligt ekstremt varme flydende metaller?


