Hvor mange hydrogenatomer er i 4,00 mol ammoniumsulfid?
1. Bestem den kemiske formel for ammoniumsulfid:
* Ammonium er NH₄⁺
* Sulfid er s²⁻
* For at afbalancere ladningerne har vi brug for to ammoniumioner for hver sulfidion:(NH₄) ₂S
2. Beregn antallet af brintatomer pr. Molekyle:
* Hver ammoniumion (NH₄⁺) har 4 hydrogenatomer.
* Formlen (NH₄) ₂S indikerer, at der er 2 ammoniumioner pr. Molekyle.
* Der er derfor 4 hydrogenatomer/ion * 2 -ioner/molekyle =8 hydrogenatomer pr. Molekyle af ammoniumsulfid.
3. Beregn det samlede antal brintatomer:
* Vi har 4,00 mol ammoniumsulfid.
* Avogadros nummer fortæller os, at der er 6,022 x 10²³ molekyler i 1 mol.
* Derfor har vi 4,00 mol * 6,022 x 10²³ molekyler/mol =2,409 x 10²⁴ molekyler af ammoniumsulfid.
* Til sidst skal du multiplicere antallet af molekyler med antallet af hydrogenatomer pr. Molekyle:2,409 x 10²⁴ molekyler * 8 hydrogenatomer/molekyle = 1,93 x 10²⁵ hydrogenatomer
Derfor er der ca. 1,93 x 10²⁵ hydrogenatomer i 4,00 mol ammoniumsulfid.
Sidste artikelHvor mange gram aluminiumhydroxid opnås fra 17,2 sulfid?
Næste artikelHvor mange atomer med brint er til stede i NH42'er?
 Varme artikler
Varme artikler
-
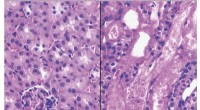 Anti-aldringsmolekylet NAD+ får et løft ved at blokere et enzymHistologisk snit af en normal nyre (venstre) versus en nyre efter akut nyreskade (højre). Kredit:J. Auwerx, EPFL Nikotinamid adenin dinukleotid (NAD+) er en vigtig spiller inden for ernæring i dag
Anti-aldringsmolekylet NAD+ får et løft ved at blokere et enzymHistologisk snit af en normal nyre (venstre) versus en nyre efter akut nyreskade (højre). Kredit:J. Auwerx, EPFL Nikotinamid adenin dinukleotid (NAD+) er en vigtig spiller inden for ernæring i dag -
 Video:Hvorfor flamingoer er sejere, end du trorKredit:The American Chemical Society For mange mennesker, flamingoer er synonyme med Florida, tarvelige plænepynt og cocktails på stranden. Men deres tåbelige ry modsiger deres utrolige overlevels
Video:Hvorfor flamingoer er sejere, end du trorKredit:The American Chemical Society For mange mennesker, flamingoer er synonyme med Florida, tarvelige plænepynt og cocktails på stranden. Men deres tåbelige ry modsiger deres utrolige overlevels -
 Ny indkapslingsteknik beskytter elektroniske egenskaber ved følsomme materialerHZDR-forskere har udviklet en ny metode til at beskytte halvledere fremstillet af følsomme materialer mod kontakt med luft og kemikalier. Det bliver, dermed, muligt at integrere disse ultratynde lag i
Ny indkapslingsteknik beskytter elektroniske egenskaber ved følsomme materialerHZDR-forskere har udviklet en ny metode til at beskytte halvledere fremstillet af følsomme materialer mod kontakt med luft og kemikalier. Det bliver, dermed, muligt at integrere disse ultratynde lag i -
 Forskere har bevist, at ozon er effektivt til at desinficere coronavirusAnbring dråber af virussuspension på sterile overflader før eksponering for ozon. Kredit:Tel Aviv Universitet Undersøgelser har vist, at SARS-CoV-2 forbliver aktiv på aerosoler og overflader i mel
Forskere har bevist, at ozon er effektivt til at desinficere coronavirusAnbring dråber af virussuspension på sterile overflader før eksponering for ozon. Kredit:Tel Aviv Universitet Undersøgelser har vist, at SARS-CoV-2 forbliver aktiv på aerosoler og overflader i mel
- Advokater sagsøger kinesiske myndigheder for ikke at slippe af med smog
- Teoretikere foreslår ny klasse af topologiske metaller med eksotiske elektroniske egenskaber
- Det er tid til at gentænke det forstyrrede amerikanske fødevaresystem fra bunden
- Kan insekter blive fede?
- Fra fladskærms -tv til din smartphone - elementet bor fortjener mere opmærksomhed
- Hvordan skriver du 0.70010 i videnskabelig notation?


