Afhænger temperaturen af et stofmasse?
* Temperatur er et mål for den gennemsnitlige kinetiske energi for molekylerne i et stof. Dette betyder, at det er et mål for, hvor meget molekylerne bevæger sig og vibrerer.
* masse er et mål for mængden af stof i et objekt.
Eksempel: Forestil dig to identiske gryder med vand, den ene med 1 liter og den anden med 2 liter. Hvis begge gryder opvarmes til den samme temperatur, vil de have den samme gennemsnitlige kinetiske energi af deres vandmolekyler, selvom en gryde indeholder flere vandmolekyler.
Der er dog nogle nuancer:
* Varmekapacitet: Mængden af varmeenergi, der kræves for at hæve temperaturen på et stof med et bestemt beløb gør afhænger af masse. Dette kaldes stoffets specifikke varmekapacitet. En større masse kræver mere varmeenergi for at nå den samme temperatur som en mindre masse.
* termisk inerti: Større genstande med større masse har en tendens til at ændre temperaturen langsommere end mindre genstande. Dette skyldes, at de har mere termisk inerti - de "modstår" ændringer i temperatur.
Kortfattet: Mens temperaturen i sig selv er uafhængig af masse, gør mængden af varmeenergi, der kræves for at ændre temperaturen på et stof , afhænger af dens masse.
Sidste artikelHvad er den ioniske karakter af bariumoxid?
Næste artikelHvad bruges natriumhydroxid og kobbersulfat til at teste for?
 Varme artikler
Varme artikler
-
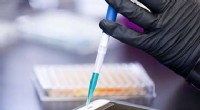 Chemist foreslår svedanalyse for bedre at sikre elektronikKemiker Jan Halámek foreslår en biometrisk-baseret tilgang til bedre at sikre elektroniske enheder. Kredit:Carlo de Jesus Jan Halámek mener, at der er en bedre metode til at sikre elektroniske enh
Chemist foreslår svedanalyse for bedre at sikre elektronikKemiker Jan Halámek foreslår en biometrisk-baseret tilgang til bedre at sikre elektroniske enheder. Kredit:Carlo de Jesus Jan Halámek mener, at der er en bedre metode til at sikre elektroniske enh -
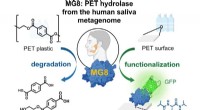 Enzym i menneskelige spytmikrober nedbryder PET-baseret plastKredit:Wiley Menneskespyt kan indeholde et enzym, som kan nedbryde plasten polyethylenterephthalat (PET). Forskere fandt det lovende enzym, en hydrolase, i en database, der indeholder prøver fra me
Enzym i menneskelige spytmikrober nedbryder PET-baseret plastKredit:Wiley Menneskespyt kan indeholde et enzym, som kan nedbryde plasten polyethylenterephthalat (PET). Forskere fandt det lovende enzym, en hydrolase, i en database, der indeholder prøver fra me -
 Usynlige organiske lysemitterende dioder når ny verdensrekordFotografi af Polytechnique Montréal-emblemet taget ved hjælp af synlig og infrarød belysning. Kredit:Pr Sébastien Kéna-Cohen Du kan ikke se det med det blotte øje, men en ny fluorescerende organis
Usynlige organiske lysemitterende dioder når ny verdensrekordFotografi af Polytechnique Montréal-emblemet taget ved hjælp af synlig og infrarød belysning. Kredit:Pr Sébastien Kéna-Cohen Du kan ikke se det med det blotte øje, men en ny fluorescerende organis -
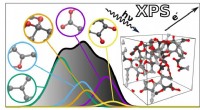 En model trænet til at forudsige spektroskopiske profiler hjælper med at tyde strukturen af mate…Den nye algoritme forudsiger XPS-spektrene for komplekse materialer baseret på individuelle atomare bidrag. Kredit:Miguel Caro / Aalto University Kulstofbaserede materialer rummer et enormt potenti
En model trænet til at forudsige spektroskopiske profiler hjælper med at tyde strukturen af mate…Den nye algoritme forudsiger XPS-spektrene for komplekse materialer baseret på individuelle atomare bidrag. Kredit:Miguel Caro / Aalto University Kulstofbaserede materialer rummer et enormt potenti
- Hvad er den bedste leder i alt metal?
- Et skridt tættere på kompleks kvanteteleportation
- En stor vulkaner med forsigtigt skrånende sider er at kalde hvad?
- Er kødfri svaret på klimaændringer?
- Hvad er de ikke -levende ressourcer, som mennesker får fra økosystemer?
- Klar til at ryste? Arktisk luft lagde Amerika på is


