Hvad er koncentrationen af en opløsning med bind 660 ml, der indeholder 33,4 gram aluminiumacetat?
1. Bestem den molære masse af aluminiumacetat
* Aluminium (AL):26,98 g/mol
* Acetat (ch₃coo⁻):59,04 g/mol
* Aluminiumacetat (AL (CH₃COO) ₃):26,98 + (3 * 59,04) =204,10 g/mol
2. Konverter massen af aluminiumacetat til mol
* Mol =masse / molær masse
* Mol =33,4 g / 204,10 g / mol =0,164 mol
3. Konverter mængden af løsning til liter
* 660 ml =0,660 L
4. Beregn koncentrationen (molaritet)
* Molaritet (m) =mol opløst / liter opløsning
* Molaritet =0,164 mol / 0,660 L =0,248 m
Derfor er koncentrationen af aluminiumacetatopløsningen 0,248 m.
 Varme artikler
Varme artikler
-
 En chip til at måle vakuumKredit:Ecole Polytechnique Federale de Lausanne Støvsugere er en vital del af de processer - såsom frysetørring - der bruges til at fremstille og konservere utallige hverdagsting og skal måles med
En chip til at måle vakuumKredit:Ecole Polytechnique Federale de Lausanne Støvsugere er en vital del af de processer - såsom frysetørring - der bruges til at fremstille og konservere utallige hverdagsting og skal måles med -
 Kunstige celler-i-celler udløst af lys fungerer som mini-kemiske reaktorerCircles in a Circle af Kandinsky. Kredit:Philadelphia Museum of Art, Louise og Walter Arensbergs Samling, 1950-134-104 Kunstige celler, der frigiver materialer, når de udsættes for lys, er blevet
Kunstige celler-i-celler udløst af lys fungerer som mini-kemiske reaktorerCircles in a Circle af Kandinsky. Kredit:Philadelphia Museum of Art, Louise og Walter Arensbergs Samling, 1950-134-104 Kunstige celler, der frigiver materialer, når de udsættes for lys, er blevet -
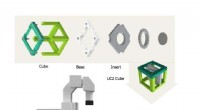 Et mikroskop for alle:Forskere udvikler open source optisk værktøjskasseDen open source 3D-printede terning kan være vært for selvdesignede indsatser, elektriske og optiske komponenter. De resulterende moduler kan kombineres til komplekse optiske instrumenter. Dette gør d
Et mikroskop for alle:Forskere udvikler open source optisk værktøjskasseDen open source 3D-printede terning kan være vært for selvdesignede indsatser, elektriske og optiske komponenter. De resulterende moduler kan kombineres til komplekse optiske instrumenter. Dette gør d -
 Tellurium gør forskellenProfessor Wolfgang Weigand fra det tyske universitet i Jena viser usædvanlige strukturer af tellurforbindelser. Kredit:Anne Günther/Uni Jena Det periodiske system indeholder 118 kemiske grundstoff
Tellurium gør forskellenProfessor Wolfgang Weigand fra det tyske universitet i Jena viser usædvanlige strukturer af tellurforbindelser. Kredit:Anne Günther/Uni Jena Det periodiske system indeholder 118 kemiske grundstoff
- Hvilken type klima har den største mængde stenforvitring forårsaget af forvitring?
- Hvorfor vil solen ikke skinne for evigt?
- Narkotikaproducenten Bristol-Myers Squibb køber Celgene for 74 milliarder dollars
- Hvad er de primære elementer i en civilisation?
- Hvilken konstellation indeholder den berømte sommerfuglklynge?
- Hvad er den pludselige bevægelse af elektriske afgifter fra et objekt til et andet?


