Er ammoniumacetat en stærk eller svag elektrolyt?
* dissociation: Når det er opløst i vand, adskiller ammoniumacetat sig i ammoniumioner (NH₄⁺) og acetationer (ch₃coo⁻). Det adskiller sig dog ikke fuldstændigt.
* ligevægt: Dissocieringsreaktionen er en ligevægtsreaktion. Dette betyder, at selvom nogle ammoniumacetat dissocierer, rekombineres nogle ioner også til dannelse af uudskilte ammoniumacetatmolekyler.
* svag syre og svag base: Ammoniumacetat dannes ved reaktionen af en svag syre (eddikesyre, ch₃cooh) og en svag base (ammoniak, NH₃). Den resulterende salt udviser svag elektrolytisk opførsel.
I modsætning hertil ville en stærk elektrolyt adskille sig næsten fuldstændigt i ioner, når de blev opløst i vand.
Fortæl mig, hvis du har flere spørgsmål!
Sidste artikelHvorfor hydrazin mere grundlæggende end ammoniak?
Næste artikelHvilken Volano er udelukkende lavet af tephra?
 Varme artikler
Varme artikler
-
 Forskere gør vitamin B12 gennembrudProfessor Martin Warren med elever fra Sir Roger Manwood School. Kredit:University of Kent Forskere ved University of Kent har gjort en betydelig opdagelse om, hvordan vitaminindholdet i nogle pla
Forskere gør vitamin B12 gennembrudProfessor Martin Warren med elever fra Sir Roger Manwood School. Kredit:University of Kent Forskere ved University of Kent har gjort en betydelig opdagelse om, hvordan vitaminindholdet i nogle pla -
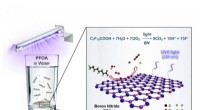 Bornitrid ødelægger for evigt kemikalier PFOA, GenXEn illustration af bornitrid-fotokatalyse, der ødelægger det forurenende stof PFOA i vand. Kredit:Billede udlånt af M. Wong/Rice University Rice University kemiingeniører fandt en effektiv katalys
Bornitrid ødelægger for evigt kemikalier PFOA, GenXEn illustration af bornitrid-fotokatalyse, der ødelægger det forurenende stof PFOA i vand. Kredit:Billede udlånt af M. Wong/Rice University Rice University kemiingeniører fandt en effektiv katalys -
 Færdiggørelse af lægemiddeldesignstikksavenKredit:University of East Anglia En kraftfuld ny måde at analysere, hvordan lægemidler interagerer med molekyler i kroppen, kan hjælpe med at designe bedre behandlinger med færre bivirkninger. De
Færdiggørelse af lægemiddeldesignstikksavenKredit:University of East Anglia En kraftfuld ny måde at analysere, hvordan lægemidler interagerer med molekyler i kroppen, kan hjælpe med at designe bedre behandlinger med færre bivirkninger. De -
 Forskere skal undersøge, om metalkorroderende mikrober kan vokse i Canadas foreslåede atomaffaldsa…Kredit:Pixabay/CC0 Public Domain Med Canada tættere på at flytte alt sit brugte nukleare brændsel til en enkelt facilitet og indkapsle hver brændstofbeholder i bentonit-ler, studerer forskere, om d
Forskere skal undersøge, om metalkorroderende mikrober kan vokse i Canadas foreslåede atomaffaldsa…Kredit:Pixabay/CC0 Public Domain Med Canada tættere på at flytte alt sit brugte nukleare brændsel til en enkelt facilitet og indkapsle hver brændstofbeholder i bentonit-ler, studerer forskere, om d
- Er det muligt for en familie med tre medlemmer at tilbringe mere på elektricitet end fem-medlemmer …
- Hvad er ledere og isolatorer af elektricitet?
- Massefylde er en målelig egenskab ved stof. Hvordan kan massefylden bestemmes?
- Autonom firbenet designet til at holde sammen med soldater
- Den officielle afslutning på alle enzymnavne?
- Hvor er Apollo 11?


