Hvad er CO2 -reaktionen med hydrazinhydrat?
Her er hvorfor:
* hydrazinhydrat er en svag base: Det kan reagere med syrer for at danne salte, men det er ikke en stærk nok base til direkte at reagere med CO2 i en simpel neutraliseringsreaktion.
* CO2 er en svag syre: Det kan reagere med baser, men det er ikke en stærk nok syre til direkte at reagere med hydrazinhydrat.
Imidlertid kan der dog ske reaktioner på specifikke forhold:
* Dannelse af hydraziniumsalte: I nærvær af vand og en katalysator kan CO2 reagere med hydrazinhydrat til dannelse af hydraziniumsalte. Disse salte er generelt ikke særlig stabile og kan nedbrydes under visse betingelser.
* nedbrydning af hydrazinhydrat: I nærvær af høje temperaturer eller stærke oxidatorer kan hydrazinhydrat nedbrydes for at frigive ammoniak (NH3) og nitrogen (N2). Den frigjorte ammoniak kan derefter reagere med CO2 for at danne ammoniumbicarbonat (NH4HCO3).
Generelt er reaktionen mellem CO2 og hydrazinhydrat kompleks og ikke ligetil. De specifikke reaktionsprodukter afhænger af reaktionsbetingelserne og tilstedeværelsen af katalysatorer.
Det er vigtigt at bemærke, at hydrazinhydrat er et meget giftigt og brandfarligt stof. Håndtering Det kræver ekstrem forsigtighed og korrekt sikkerhedsforholdsregler.
Sidste artikelHvad hedder CO8 CO8?
Næste artikelHvordan illustrerer hydrazin og ammoniak loven i flere proportioner?
 Varme artikler
Varme artikler
-
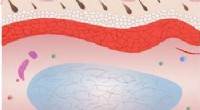 Hydrogel heler uden tilsætningsstofferEn illustration viser, hvordan over seks uger, fra top til bund, en hydrogel, der er udviklet ved Rice University, hjælper med vævsremodellering. Processen begynder med celleinfiltration efterfulgt af
Hydrogel heler uden tilsætningsstofferEn illustration viser, hvordan over seks uger, fra top til bund, en hydrogel, der er udviklet ved Rice University, hjælper med vævsremodellering. Processen begynder med celleinfiltration efterfulgt af -
 Kunne ungt blod holde hemmeligheder længere, sundere liv?Kredit:offentligt domæne I det der lyder som en scene fra en science fiction -film, forskere i 2005 syede gamle og unge mus sammen, så de delte et kredsløbssystem. Ungdommeligt blod foryngede tils
Kunne ungt blod holde hemmeligheder længere, sundere liv?Kredit:offentligt domæne I det der lyder som en scene fra en science fiction -film, forskere i 2005 syede gamle og unge mus sammen, så de delte et kredsløbssystem. Ungdommeligt blod foryngede tils -
 Vågn op og duft til kaffen:Forskning viser, at frysebønner kan bevare aromaenAndrew Cotter demonstrerer den projektive kortlægningsøvelse, der blev brugt i hans forskning. De mørktonede vinglas indeholder de forskellige malede kaffer, der blev brugt i undersøgelsen. Kredit:Pen
Vågn op og duft til kaffen:Forskning viser, at frysebønner kan bevare aromaenAndrew Cotter demonstrerer den projektive kortlægningsøvelse, der blev brugt i hans forskning. De mørktonede vinglas indeholder de forskellige malede kaffer, der blev brugt i undersøgelsen. Kredit:Pen -
 Ny teknik muliggør real-time mikroskopi ved høj varme og belastningEt kig inde i in situ scanning elektronmikroskopi varme- og indlæsningsenhed. Kredit:North Carolina State University Forskere har demonstreret en teknik, der giver dem mulighed for at spore mikros
Ny teknik muliggør real-time mikroskopi ved høj varme og belastningEt kig inde i in situ scanning elektronmikroskopi varme- og indlæsningsenhed. Kredit:North Carolina State University Forskere har demonstreret en teknik, der giver dem mulighed for at spore mikros
- Hvad er aeolisk energi?
- Antarktis ishylde synger, mens vinden pisker hen over dens overflade
- 433 personer vinder en jackpot i lotteriet. Umulig? Sandsynlighed og psykologi tyder på, at det er …
- Bestyrelsesmedlemmer med ø-skattely-bånd signalerer større niveauer af skatteundgåelse, undersø…
- Hvad er arten af bushfires i Australien?
- Hvor længe for månelyset når jorden?


