Hvad er den elektroniske konfiguration til calciumchlorid?
* calcium (CA): Calcium er i gruppe 2, så det har 2 valenselektroner. Det mister disse elektroner til at danne en +2 -kation.
* Neutral calcium:1S² 2S² 2P⁶ 3S² 3P⁶ 4S²
* Calciumion (Ca²⁺):1S² 2S² 2P⁶ 3S² 3P⁶
* klor (Cl): Klor er i gruppe 17, så det har 7 valenselektroner. Det får en elektron til dannelse af en -1 -anion.
* Neutral klor:1S² 2S² 2p⁶ 3S² 3P⁵
* Chloridion (CL⁻):1S² 2S² 2P⁶ 3S² 3P⁶
Derfor er de elektroniske konfigurationer til ionerne i calciumchlorid:
* ca²⁺: 1S² 2S² 2P⁶ 3S² 3P⁶
* cl⁻: 1S² 2S² 2P⁶ 3S² 3P⁶
 Varme artikler
Varme artikler
-
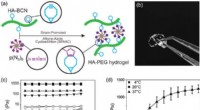 3-D dyrkning af hepatocytter på en lever-på-en-chip-enhed(a) Skematisk repræsentation af dannelsen af HA-PEG-hydrogeler gennem en stamme-promoveret alkyn-azid-cycloadditionsreaktion. (b) Fotografi af en HA-PEG hydrogel efter dannelse. (c) Frekvenssweep af
3-D dyrkning af hepatocytter på en lever-på-en-chip-enhed(a) Skematisk repræsentation af dannelsen af HA-PEG-hydrogeler gennem en stamme-promoveret alkyn-azid-cycloadditionsreaktion. (b) Fotografi af en HA-PEG hydrogel efter dannelse. (c) Frekvenssweep af -
 Nikkel i røntgenlysetForskere fra Argonne og University of California i Santa Barbara har identificeret en anden elementær aktør, der hjælper med at aktivere palladium og samtidig reducere mængden af det ædle metal, der
Nikkel i røntgenlysetForskere fra Argonne og University of California i Santa Barbara har identificeret en anden elementær aktør, der hjælper med at aktivere palladium og samtidig reducere mængden af det ædle metal, der -
 Teamet udvikler metode til neurale netberegninger i vandEt ionisk kredsløb, der omfatter hundredvis af ioniske transistorer. Kredit:Woo-Bin Jung/Harvard SEAS Mikroprocessorer i smartphones, computere og datacentre behandler information ved at manipulere
Teamet udvikler metode til neurale netberegninger i vandEt ionisk kredsløb, der omfatter hundredvis af ioniske transistorer. Kredit:Woo-Bin Jung/Harvard SEAS Mikroprocessorer i smartphones, computere og datacentre behandler information ved at manipulere -
 Grøn kemi og biobrændstof:Mekanismen for et centralt fotoenzym dekrypteretKunstnerindtryk af den enzymatiske katalyse foreslået i mekanisme af fedtsyrefotodecarboxylase. Kredit:Damien Sorigué Funktionen af enzymet FAP, nyttig til produktion af biobrændstoffer og til g
Grøn kemi og biobrændstof:Mekanismen for et centralt fotoenzym dekrypteretKunstnerindtryk af den enzymatiske katalyse foreslået i mekanisme af fedtsyrefotodecarboxylase. Kredit:Damien Sorigué Funktionen af enzymet FAP, nyttig til produktion af biobrændstoffer og til g


