Hvorfor sølvchlorid bliver gråt i sollys?
Her er sammenbruddet:
* sollys energi: Sollys indeholder ultraviolet (UV) stråling, der bærer nok energi til at bryde den kemiske binding mellem sølv og klor i sølvchlorid.
* Nedbrydning: Når AGCL absorberer UV-lys, får energien, at chloridionerne (CL-) frigives som klorgas (CL2), hvilket efterlader sølvmetal (Ag).
* farveændring: Sølvmetal er grå i farve, hvilket resulterer i den observerede grå misfarvning af sølvchloridet.
Reaktionen kan repræsenteres af følgende ligning:
2agcl (s) → 2ag (s) + cl2 (g)
Faktorer, der påvirker misfarvningsgraden:
* intensitet af sollys: Stærkere UV -stråling fører til hurtigere nedbrydning.
* tilstedeværelse af urenheder: Nogle urenheder kan fungere som katalysatorer og fremskynde processen.
* Temperatur: Højere temperaturer fremskynder generelt kemiske reaktioner.
Bemærk: Dette er grunden til, at sølvchlorid bruges til fotografering. De lysfølsomme krystaller udsættes for lys, hvilket forårsager nedbrydning af sølvchlorid. Mængden af lys, der rammer hver del af filmen, bestemmer mængden af sølvmetal, der er dannet, hvilket resulterer i et fotografisk billede.
Sidste artikelHvad er den sammensatte P3O5?
Næste artikelDen energi, der kræves for at bryde bindingerne i 1 mol af en kemisk forbindelse?
 Varme artikler
Varme artikler
-
 ABS af molekylære motorerHarald Platta, Rebecca Brinkmeier og Thomas Mastalski (fra venstre) i laboratoriet på Ruhr-Universität Bochum. Kredit:RUB, Kramer Peroxisomer er celleorganeller, der udfører en række funktioner, h
ABS af molekylære motorerHarald Platta, Rebecca Brinkmeier og Thomas Mastalski (fra venstre) i laboratoriet på Ruhr-Universität Bochum. Kredit:RUB, Kramer Peroxisomer er celleorganeller, der udfører en række funktioner, h -
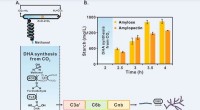 Kinesiske videnskabsmænd rapporterer om stivelsesyntese fra kuldioxidStivelsessyntese via kunstig stivelse anabolsk vej (ASAP) fra kuldioxid. Kredit:TIBCAS Kinesiske videnskabsmænd rapporterede for nylig om en de novo-rute til kunstig stivelsessyntese fra kuldioxid
Kinesiske videnskabsmænd rapporterer om stivelsesyntese fra kuldioxidStivelsessyntese via kunstig stivelse anabolsk vej (ASAP) fra kuldioxid. Kredit:TIBCAS Kinesiske videnskabsmænd rapporterede for nylig om en de novo-rute til kunstig stivelsessyntese fra kuldioxid -
 En katalysator, der ødelægger perklorat i vand, kan rense MarsjordKredit:CC0 Public Domain Ateam ledet af UC Riverside-ingeniører har udviklet en katalysator til at fjerne et farligt kemikalie fra vand på Jorden, der også kan gøre Marsjord mere sikker for landbr
En katalysator, der ødelægger perklorat i vand, kan rense MarsjordKredit:CC0 Public Domain Ateam ledet af UC Riverside-ingeniører har udviklet en katalysator til at fjerne et farligt kemikalie fra vand på Jorden, der også kan gøre Marsjord mere sikker for landbr -
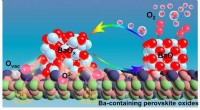 Mekanisme for oxygenaktivering på bariumholdige perovskitmaterialerOxygenaktiveringsmekanisme på Ba-holdige perovskitoxider. Kredit:Zhu Yue Et forskerhold ledet af prof. Yang Weishen og prof. Zhu Xuefeng fra Dalian Institute of Chemical Physics (DICP) fra det kine
Mekanisme for oxygenaktivering på bariumholdige perovskitmaterialerOxygenaktiveringsmekanisme på Ba-holdige perovskitoxider. Kredit:Zhu Yue Et forskerhold ledet af prof. Yang Weishen og prof. Zhu Xuefeng fra Dalian Institute of Chemical Physics (DICP) fra det kine
- Hvorfor sol er stjerne?
- Hvorfor betragtes asteroider meteoroider kometer og støv som en del af vores solsystem?
- Fjern 'rumsnemand' låser op for mysteriet om, hvordan nogle sovende dybe rumobjekter bliver til 'is…
- Er Venus i sin fulde fase synlig fra Jorden?
- Hvilken type sygdom er tyfus?
- Hvad er et femtosekund i Hertz?


