Hvad kan du observere, når natrium og klor reagerer?
Visuelle observationer:
* kraftig reaktion: Reaktionen er meget eksoterm, hvilket betyder, at den frigiver en betydelig mængde varme.
* lys orange-gul flamme: Reaktionen producerer en lys orange-gul flamme som et resultat af de ophidsede natriumatomer, der udsender lys.
* hvid røg: Fin hvid røg, som faktisk er små partikler af fast natriumchlorid, produceres, når reaktionen skrider frem.
* Dannelse af et hvidt fast stof: Den hvide røg sætter sig til sidst ned som en hvid fast masse, som er natriumchlorid.
Kemiske observationer:
* Ændring i egenskaber: Reaktionen involverer den komplette ændring af reaktanternes egenskaber. Natrium, et blødt, sølvfarvet metal og klor, en grøn-gul gas, kombineres for at danne et hvidt, krystallinsk fast stof.
* ionisk binding: Reaktionen danner en ionisk binding mellem natrium- og kloratomer. Natriumatomet mister et elektron til dannelse af en positivt ladet ion (Na+), og kloratomet får et elektron til dannelse af en negativt ladet ion (CL-). Disse modsatte ladede ioner tiltrækkes af hinanden og danner den stabile natriumchloridforbindelse.
sikkerhed:
* FORSIGTIG: Denne reaktion er meget eksoterm og bør udføres med ekstrem forsigtighed. Det er bedst at observere denne reaktion demonstreret af en uddannet professionel i et sikkert miljø.
* Sikkerhedsudstyr: Passende sikkerhedsudstyr, inklusive beskyttelsesbriller og handsker, skal altid bruges, når disse stoffer håndterer.
Kortfattet:
Reaktionen mellem natrium og klor er en dramatisk og visuelt spændende kemisk reaktion, der demonstrerer dannelsen af en ionisk forbindelse og frigivelse af betydelig energi.
Sidste artikelHvilken ville korrodere første kobber eller jern?
Næste artikelHvordan adskiller du klor fra salt?
 Varme artikler
Varme artikler
-
 Fyrrenåle fra gamle juletræer kan i fremtiden blive til maling og sødemidlerKredit:CC0 Public Domain Forladte juletræer kunne reddes fra losseplads og omdannes til maling og sødemidler til mad ifølge ny forskning fra University of Sheffield. Juletræer har hundredtusindvi
Fyrrenåle fra gamle juletræer kan i fremtiden blive til maling og sødemidlerKredit:CC0 Public Domain Forladte juletræer kunne reddes fra losseplads og omdannes til maling og sødemidler til mad ifølge ny forskning fra University of Sheffield. Juletræer har hundredtusindvi -
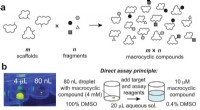 Store antal makrocykliske forbindelser, der er nødvendige for at udvikle lægemidler mod vanskelige…Diversificering af makrocykliske stilladser ved kombinatorisk at tilføje fragmenter til perifere grupper. et generelt princip for tilgangen. b Billede af en 80 nL dråbe overført af ADE, vist i en 96-b
Store antal makrocykliske forbindelser, der er nødvendige for at udvikle lægemidler mod vanskelige…Diversificering af makrocykliske stilladser ved kombinatorisk at tilføje fragmenter til perifere grupper. et generelt princip for tilgangen. b Billede af en 80 nL dråbe overført af ADE, vist i en 96-b -
 Ny brug af NMR kaster lys over elektropolymeriserede katalysatorer, der er nemme at fremstilleSEM-billeder (×30k) af PANI (a) og PASP (b) tynde film dyrket på GCEer. Kredit:American Institute of Physics I en verden af katalytiske reaktioner, polymerer skabt gennem elektropolymerisation t
Ny brug af NMR kaster lys over elektropolymeriserede katalysatorer, der er nemme at fremstilleSEM-billeder (×30k) af PANI (a) og PASP (b) tynde film dyrket på GCEer. Kredit:American Institute of Physics I en verden af katalytiske reaktioner, polymerer skabt gennem elektropolymerisation t -
 En ny måde at se, om der er genbrugsmateriale i den plastikflaske eller -poseTilføjelse af et fluorescerende mærke til genbrugsplast kan hjælpe med at spore deres mængde i nye engangsprodukter. Kredit:Tilpasset fra ACS Sustainable Chemistry &Engineering 2022 For at tilskynd
En ny måde at se, om der er genbrugsmateriale i den plastikflaske eller -poseTilføjelse af et fluorescerende mærke til genbrugsplast kan hjælpe med at spore deres mængde i nye engangsprodukter. Kredit:Tilpasset fra ACS Sustainable Chemistry &Engineering 2022 For at tilskynd
- Billig billedbehandlingssystem klar til at give automatisk myggesporing
- Hvad er de tre måder, din krop bruger energi hver dag på?
- Video:Cassini-Huygens historiske eventyr
- Hvilket metal har en masse på 61,0 og rumfanget 5,40?
- Hvor meget energi genererer vindmøller?
- Ny internet of things-protokol til at transformere hoteloplevelsen


