Hvilken ændring i elektronstruktur forekommer, når et natriumatom bliver ion?
natriumatom (NA)
* Elektronkonfiguration: 1S² 2S² 2P⁶ 3S¹
* Valenselektroner: 1 (den ensomme elektron i 3'erne orbital)
natriumion (Na+)
* Elektronkonfiguration: 1S² 2S² 2P⁶
* Valenselektroner: 0
ændringen
Når et natriumatom bliver en natriumion (Na+), mister det sin enkelt valenselektron . Dette elektron doneres til et andet atom, typisk en ikke -metal, for at danne en ionisk binding. Tabet af denne elektron efterlader natriumionen med en fuld ydre skal (2p -skallen), hvilket gør den mere stabil.
Nøglepunkter
* stabilitet: Ioner er mere stabile end deres tilsvarende neutrale atomer, fordi de har en fuld ydre skal af elektroner.
* opladning: At miste en elektron giver natriumionen en positiv ladning (+1), da der nu er flere protoner end elektroner.
* octet regel: Natrium opnår sin elektron ved at miste sin elektron en stabil elektronkonfiguration som Noble Gas Neon (NE), der opfylder Octet -reglen.
Sidste artikelHvis pH er 3, hvad koncentrationen af brint?
Næste artikelHvad ville reaktionen med fluor og natrium være?
 Varme artikler
Varme artikler
-
 Forskere udvikler hurtig kemi, der låser op for en ny klasse af polymererForskere har udviklet en kemisk proces, der kan gøre en klasse af polymerer kendt som polysulfater mere konkurrencedygtige med polycarbonater - robust plast, der kan danne strukturelle paneler som dem
Forskere udvikler hurtig kemi, der låser op for en ny klasse af polymererForskere har udviklet en kemisk proces, der kan gøre en klasse af polymerer kendt som polysulfater mere konkurrencedygtige med polycarbonater - robust plast, der kan danne strukturelle paneler som dem -
 Grøn funktionalisering af kulstof-brintbindingerProf Wu og hans medarbejdere diskuterer organiske molekylære transformationsprocesser i deres laboratorium. De har udviklet en grøn proces, som gør brug af lys til at funktionalisere organiske molekyl
Grøn funktionalisering af kulstof-brintbindingerProf Wu og hans medarbejdere diskuterer organiske molekylære transformationsprocesser i deres laboratorium. De har udviklet en grøn proces, som gør brug af lys til at funktionalisere organiske molekyl -
 Konstruerede bakterier udskiller kræftbiomarkørerEscherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH Skam med glycanen - disse komplekse sukkermolekyler er knyttet til 80% af proteinerne i den menneskelige krop, gør dem til en væsen
Konstruerede bakterier udskiller kræftbiomarkørerEscherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH Skam med glycanen - disse komplekse sukkermolekyler er knyttet til 80% af proteinerne i den menneskelige krop, gør dem til en væsen -
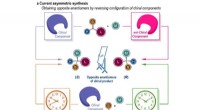 Forskere får adgang til begge enantiomerer efter varierende reaktionstidFigur 1. Strategier til opnåelse af begge enantiomerer af chirale molekyler. Kredit:SIOC Homokiralitet er et grundlæggende træk ved alle levende organismer. Det er velkendt, at et par enantiomerer
Forskere får adgang til begge enantiomerer efter varierende reaktionstidFigur 1. Strategier til opnåelse af begge enantiomerer af chirale molekyler. Kredit:SIOC Homokiralitet er et grundlæggende træk ved alle levende organismer. Det er velkendt, at et par enantiomerer
- Støjforurening viste sig at være forstyrrende for skolegang af fisk
- NASA finder tropiske depressionsknopper regne over Mexico
- Hvad er atmosfæren i Jupiter lavet af?
- Differentiere kørselslængdekodning og cellekodning?
- Hvad er nogle vigtige geologiske træk ved Nagasaki?
- Sådan ændres farven på en bålflamme


