Hvordan vil du retfærdiggøre, at vand er en forbindelse?
* Fast sammensætning: Vand består altid af to hydrogenatomer og et iltatom, repræsenteret af den kemiske formel H₂O. Dette faste forhold mellem elementer er et definerende kendetegn for forbindelser.
* Forskellige egenskaber: Vand har tydeligt forskellige egenskaber sammenlignet med dets bestanddele, brint og ilt. Hydrogen er en brandfarlig gas, mens ilt er en farveløs og lugtfri gas. Vand er en væske ved stuetemperatur, har et højt kogepunkt og er vigtigt for livet.
* Kemisk reaktion: Vand dannes af en kemisk reaktion mellem brint og ilt. Denne reaktion involverer brud og dannelse af kemiske bindinger, hvilket resulterer i et nyt stof med forskellige egenskaber.
* Nedbrydning: Vand kan opdeles i dets bestanddele (brint og ilt) gennem elektrolyse, en proces, der kræver energi for at bryde de kemiske bindinger, der holder forbindelsen sammen.
På grund af dens faste sammensætning opfylder der derfor forskellige egenskaber, dannelse gennem en kemisk reaktion og evnen til at nedbrydes i dens elementer, der endeligt er kriterierne for en forbindelse.
 Varme artikler
Varme artikler
-
 Biostasis har til formål at forhindre død efter traumatisk skade ved at bremse biokemiske reaktion…DARPAs Biostasis-program har til formål at forhindre død efter traumatisk skade ved at bremse biokemiske reaktioner inde i celler, dermed forlænge den gyldne time for medicinsk intervention. De ønsked
Biostasis har til formål at forhindre død efter traumatisk skade ved at bremse biokemiske reaktion…DARPAs Biostasis-program har til formål at forhindre død efter traumatisk skade ved at bremse biokemiske reaktioner inde i celler, dermed forlænge den gyldne time for medicinsk intervention. De ønsked -
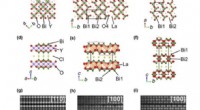 Teambilledressourcer brugt i internationalt eksperiment med nye fotokatalysatorerKredit:Skolkovo Institut for Videnskab og Teknologi Skoltech-forskere hjalp deres kolleger fra Japan, Tyskland, De Forenede Stater, og Kina studerer krystalstrukturen og optiske egenskaber af en n
Teambilledressourcer brugt i internationalt eksperiment med nye fotokatalysatorerKredit:Skolkovo Institut for Videnskab og Teknologi Skoltech-forskere hjalp deres kolleger fra Japan, Tyskland, De Forenede Stater, og Kina studerer krystalstrukturen og optiske egenskaber af en n -
 Billeddannelse på atomniveau kunne tilbyde en køreplan for metaller med nye egenskaberDenne skematiske illustration af den nye palladiumholdige højentropi tillader viser, hvordan ny legering indeholder store palladiumklynger (blå atomer). Kredit:Ting Zhu Højentropi legeringer, som
Billeddannelse på atomniveau kunne tilbyde en køreplan for metaller med nye egenskaberDenne skematiske illustration af den nye palladiumholdige højentropi tillader viser, hvordan ny legering indeholder store palladiumklynger (blå atomer). Kredit:Ting Zhu Højentropi legeringer, som -
 Fra bronzealderen til maddåser, her er hvordan tin ændrede menneskehedenTin kommer fra malmen cassiterit. Kredit:Shutterstock/PYP Nævn tin, og de fleste mennesker ville tænke på den typiske blikdåse, bruges til at konservere fødevarer, du opbevarer i dine skabe. Tin b
Fra bronzealderen til maddåser, her er hvordan tin ændrede menneskehedenTin kommer fra malmen cassiterit. Kredit:Shutterstock/PYP Nævn tin, og de fleste mennesker ville tænke på den typiske blikdåse, bruges til at konservere fødevarer, du opbevarer i dine skabe. Tin b
- Forskning afslører, hvorfor folk vælger bestemte campingpladser
- Diamanter anvender både optisk mikroskopi og MR for bedre billeddannelse
- Fjernstyrede havdroner observerer atmosfæriske kolde pools
- Livet på velfærd er ikke, hvad de fleste mennesker tror, det er
- Hvorfor atomenergi bør være en del af Afrikas energimix
- Hvordan gives en underart videnskabeligt navn?


