Et stof, der danner hydroxidioner?
Her er en sammenbrud:
* Arrhenius Definition: En base er et stof, der producerer hydroxidioner (OH-), når det opløses i vand.
* Brønsted-Lowry Definition: En base er et stof, der accepterer en proton (H+). Denne definition er bredere og inkluderer stoffer, der ikke nødvendigvis indeholder hydroxidioner.
* Lewis Definition: En base er en elektronpar -donor.
Eksempler på almindelige baser inkluderer:
* metalhydroxider: NaOH (natriumhydroxid), KOH (kaliumhydroxid), Ca (OH) ₂ (calciumhydroxid)
* ammoniak (NH₃): Dette fungerer som en base ved at acceptere en proton fra vand til dannelse af ammoniumioner (NH₄+) og hydroxidioner.
* Mange organiske forbindelser: For eksempel kan aminer som methylamin (CH₃NH₂) acceptere en proton til dannelse af en positivt ladet ammoniumion.
Fortæl mig, hvis du gerne vil udforske nogen af disse koncepter mere detaljeret!
 Varme artikler
Varme artikler
-
 Resonansforbedret tunneling inducerer flour- og para-hydrogenreaktion i interstellare skyerDe høje søjler og runde kugler af mørkt støv og kold molekylær gas i stjerneskyer Kredit:T. A. Rector &B. A. Wolpa, NOAO, AURA Forskere fra Dalian Institute of Chemical Physics (DICP) fra det kine
Resonansforbedret tunneling inducerer flour- og para-hydrogenreaktion i interstellare skyerDe høje søjler og runde kugler af mørkt støv og kold molekylær gas i stjerneskyer Kredit:T. A. Rector &B. A. Wolpa, NOAO, AURA Forskere fra Dalian Institute of Chemical Physics (DICP) fra det kine -
 Indbygget gassensorenhed lover enkel, nøjagtig påvisning af flygtige organiske forbindelserI gennemgang af videnskabelige instrumenter, forskere ved Gdańsk University of Technology beskriver en måleanordning designet til at analysere luftprøver indeholdende forskellige flygtige organiske fo
Indbygget gassensorenhed lover enkel, nøjagtig påvisning af flygtige organiske forbindelserI gennemgang af videnskabelige instrumenter, forskere ved Gdańsk University of Technology beskriver en måleanordning designet til at analysere luftprøver indeholdende forskellige flygtige organiske fo -
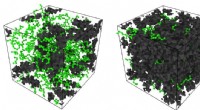 Tæt mellemrum spids tilstedeværelse af petrokemikalierSimuleringssnapshots af Rice University-ingeniører viser n-heptan-molekyler (grøn) under forskellige grader af indeslutning i en polymermatrix af molekyler (sort), hvor den højviskose polymer er en mo
Tæt mellemrum spids tilstedeværelse af petrokemikalierSimuleringssnapshots af Rice University-ingeniører viser n-heptan-molekyler (grøn) under forskellige grader af indeslutning i en polymermatrix af molekyler (sort), hvor den højviskose polymer er en mo -
 Tweaks bag genfødslen af næsten kasserede organiske solteknologierUdvælgelse af solceller i laboratoriet hos GTRI Principal Research Engineer Jud Ready. Cellerne inkluderer 3D, CZTS, organisk solcelle, og silicium. Kredit:Georgia Tech/Branden Camp Et solenergima
Tweaks bag genfødslen af næsten kasserede organiske solteknologierUdvælgelse af solceller i laboratoriet hos GTRI Principal Research Engineer Jud Ready. Cellerne inkluderer 3D, CZTS, organisk solcelle, og silicium. Kredit:Georgia Tech/Branden Camp Et solenergima


