Hvordan adskiller den molekylære formel ikke sig fra N2O?
nej (nitrogenoxid):
* sammensætning: Ét nitrogenatom (N) og et iltatom (O).
* egenskaber: En farveløs gas, meget reaktiv, spiller en rolle i biologiske processer og atmosfærisk kemi.
N2O (nitrogenoxid):
* sammensætning: To nitrogenatomer (N) og et iltatom (O).
* egenskaber: Også en farveløs gas, men mindre reaktiv end nej. Almindeligvis kendt som lattergas, der bruges som bedøvelsesmiddel og i piskede fløde dåser.
Nøgleforskelle:
* Antal atomer: Ingen har et nitrogen og et iltatom, mens N2O har to nitrogen og et iltatom.
* molekylvægt: NO har en molekylvægt på 30 g/mol, mens N2O har en molekylvægt på 44 g/mol.
* Kemiske egenskaber: Nej er meget reaktiv på grund af et uparret elektron, mens N2O er mindre reaktiv.
* biologiske og industrielle anvendelser: Ingen spiller en rolle i blodkarudvidelse og andre biologiske processer. N2O bruges som bedøvelsesmiddel og i piskede flødebeholdere.
I resumé ligger forskellen mellem NO og N2O i antallet af atomer i hvert element, hvilket resulterer i forskellige molekylvægte og kemiske egenskaber, hvilket fører til forskellige anvendelser inden for forskellige felter.
Sidste artikelHvad er sandt med elektronerne i en svovlion?
Næste artikelHvad sker der, når natriumphosphat blandes med kobbersulfat?
 Varme artikler
Varme artikler
-
 Vurdering af batteriydelse:Sammenlignet med hvad?Testfacilitet til evaluering af batteriydelse og levetid på Argonne National Laboratory. Kredit:Argonne National Laboratory Forskere må ofte spørge sig selv, i forhold til hvad? Hvordan er de resu
Vurdering af batteriydelse:Sammenlignet med hvad?Testfacilitet til evaluering af batteriydelse og levetid på Argonne National Laboratory. Kredit:Argonne National Laboratory Forskere må ofte spørge sig selv, i forhold til hvad? Hvordan er de resu -
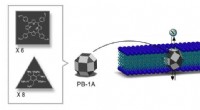 Syntetiske nanokanaler til jodidtransport3-D struktur af den syntetiske iodid-transporter PB-1A udviklet af IBS forskere. PB-1A-design følger formen af 26-sidet polyeder lavet af trekanter og firkanter (mørkegrå) med 12 flader efterladt to
Syntetiske nanokanaler til jodidtransport3-D struktur af den syntetiske iodid-transporter PB-1A udviklet af IBS forskere. PB-1A-design følger formen af 26-sidet polyeder lavet af trekanter og firkanter (mørkegrå) med 12 flader efterladt to -
 IcePic-algoritmen klarer sig bedre end mennesker i at forudsige iskrystaldannelseEn repræsentation af de mange forskellige materialer, der undersøges for deres potentiale til at kontrollere isdannelse. Kredit:Michael B. Davies Cambridge-forskere har udviklet en kunstigt intelli
IcePic-algoritmen klarer sig bedre end mennesker i at forudsige iskrystaldannelseEn repræsentation af de mange forskellige materialer, der undersøges for deres potentiale til at kontrollere isdannelse. Kredit:Michael B. Davies Cambridge-forskere har udviklet en kunstigt intelli -
 Befugtende ejendom af Li metal med grafitKontaktvinkeleksperimenter af Li-metal og grafitmaterialer:(a-c) stærkt orienteret pyrolytisk grafit (HOPG); (d-f) porøst carbonpapir (PCP); (g-i) lithieret porøst carbonpapir (litieret PCP). Kredit:©
Befugtende ejendom af Li metal med grafitKontaktvinkeleksperimenter af Li-metal og grafitmaterialer:(a-c) stærkt orienteret pyrolytisk grafit (HOPG); (d-f) porøst carbonpapir (PCP); (g-i) lithieret porøst carbonpapir (litieret PCP). Kredit:©
- Hvis et objekt accelererer i samme retning, som det bevæger sig, hvordan hastighed påvirkes?
- Hvordan ser store sletter ud?
- Påvirker lufttrykket opløsning af krystaller?
- Fugle, der spiser fyrretræskræfrø
- Hvad er de tekniske overvejelser for stødende sedimentære og metamorfe klipper?
- Hvad gør KT Tape? Hvordan Kinesio Tape virker


