Hvilken teknik skal bruges, når der ændrer noget kobbersulfatopløsning til fast sulfat?
Hvorfor fordampning?
* opløselighed: Kobbersulfat er et meget opløseligt salt i vand. Dette betyder, at det let opløses og danner en klar blå opløsning.
* Krystallisation: Når vandet fordamper, øges koncentrationen af kobbersulfat i opløsningen. Til sidst bliver opløsningen overmættet, hvilket betyder, at den indeholder mere opløst stof, end den normalt kan opløses. Dette får kobbersulfatet til at krystallisere ud af opløsningen som faste krystaller.
Procedure:
1. Start med kobbersulfatopløsningen: Du har brug for en opløsning af kobbersulfat.
2. Varm forsigtigt: Opvarmes opløsningen forsigtigt i en passende beholder (som et bægerglas eller fordampningsskål). Du kan bruge en Bunsen -brænder, en varmplade eller en varmelampe. Målet er at fordampe vandet uden at koge det for kraftigt, hvilket kan forårsage spredning.
3. Overvåg fordampningen: Når vandet fordamper, vil opløsningen blive mere koncentreret, og farven bliver mere intens. Se nøje.
4. Krystaldannelse: Når opløsningen bliver tilstrækkelig koncentreret, ser du små blå krystaller af kobbersulfat begynder at dannes på bunden og siderne af beholderen.
5. Fortsæt fordampning: Fortsæt med at opvarme forsigtigt, indtil det meste af vandet er fordampet, og du har en betydelig mængde af faste kobbersulfatkrystaller.
6. Tillad at køle: Når krystallerne er dannet, skal du lade beholderen afkøle til stuetemperatur. Dette vil hjælpe krystalerne med at styrke yderligere.
7. indsamle og tørre (valgfrit): Du kan omhyggeligt hælde enhver resterende væske og derefter tørre krystallerne på et varmt, tørt sted.
Vigtige noter:
* sikkerhed: Brug altid passende beskyttelsesbriller og handsker, når du arbejder med kemikalier.
* varmekontrol: Opvarm ikke opløsningen for hurtigt, da dette kan få opløsningen til at sprøjte.
* renhed: Renheden af kobbersulfatkrystaller afhænger af renheden af startopløsningen, og hvor omhyggeligt du fordamper vandet.
Fortæl mig, hvis du har flere spørgsmål!
 Varme artikler
Varme artikler
-
 Heterogen ethylenhydroformylering muliggør højeffektiv industriel produktion af propanal/n-propano…Den industrielle facilitet med 50 kt/år propanal/n-propanol ved heterogen ethylenhydroformylering. Kredit:LI Cunyao Olefiner, hydrogen og carbonmonoxid kan omdannes til aldehyder ved hydroformyleri
Heterogen ethylenhydroformylering muliggør højeffektiv industriel produktion af propanal/n-propano…Den industrielle facilitet med 50 kt/år propanal/n-propanol ved heterogen ethylenhydroformylering. Kredit:LI Cunyao Olefiner, hydrogen og carbonmonoxid kan omdannes til aldehyder ved hydroformyleri -
 Ny tilgang letter spektroskopi på individuelle molekylerProfessor Dr. Juergen Hauer (tv) og førsteforfatter Erling Thyrhaug med deres måleinstrument. I baggrunden, spektre taget med. Kredit:Andreas Battenberg Mens spektroskopiske målinger normalt bereg
Ny tilgang letter spektroskopi på individuelle molekylerProfessor Dr. Juergen Hauer (tv) og førsteforfatter Erling Thyrhaug med deres måleinstrument. I baggrunden, spektre taget med. Kredit:Andreas Battenberg Mens spektroskopiske målinger normalt bereg -
 Forskere analyserer, hvordan 3-D-printede metaller bryderTomografi rekonstruktion af en aluminiumslegering fremstillet ved hjælp af 3D-printteknikker (mikrohulrum er farvet orange). Kredit:Universidad Carlos III de Madrid 3-D-printede metaller er blevet
Forskere analyserer, hvordan 3-D-printede metaller bryderTomografi rekonstruktion af en aluminiumslegering fremstillet ved hjælp af 3D-printteknikker (mikrohulrum er farvet orange). Kredit:Universidad Carlos III de Madrid 3-D-printede metaller er blevet -
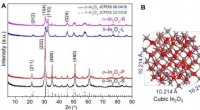 Effektive indiumoxidkatalysatorer designet til CO2-hydrogenering til methanolKredit:Chinese Academy of Sciences Katalytisk hydrogenering af kuldioxid (CO 2 ) er et grønt og bæredygtigt middel til at syntetisere råvarekemikalier såsom methanol. Denne konverteringsproces e
Effektive indiumoxidkatalysatorer designet til CO2-hydrogenering til methanolKredit:Chinese Academy of Sciences Katalytisk hydrogenering af kuldioxid (CO 2 ) er et grønt og bæredygtigt middel til at syntetisere råvarekemikalier såsom methanol. Denne konverteringsproces e
- Hvad er formlen for forbindelse dannet mellem ioner F- og CR2 plus plus?
- Offentligheden opfordres til at hjælpe med at løse mysteriet om, hvorfor et af Storbritanniens mes…
- Sådan ser man kometen Leonard, ifølge den forsker, der opdagede den
- Discovery hjælper med at forbedre nøjagtigheden af CRISPR-Cas9-genredigering
- Hvordan kan man identificere en måne -meteorit?
- Global opvarmning tegner sig for tredobling af ekstreme vestafrikanske Sahel-storme, viser undersøg…


