Hvad er den kemiske reaktionstype, når bly II -nitrat blandet med kaliumiodid?
Her er hvorfor:
* dobbeltfortrængningsreaktioner involverer udveksling af ioner mellem to reaktanter. I dette tilfælde kombineres bly (II) -ioner (Pb²⁺) fra bly (II) nitrat med iodidionerne (I⁻) fra kaliumiodid til dannelse af bly (II) iodid (PBI₂), som er et gult bundfald.
* De resterende ioner, kalium (K⁺) og nitrat (NO₃⁻), kombineres også for at danne kaliumnitrat (Kno₃), som forbliver opløst i opløsning.
Den afbalancerede kemiske ligning for denne reaktion er:
Pb (no₃) ₂ (aq) + 2 ki (aq) → pbi₂ (s) + 2 kno₃ (aq)
Her er en sammenbrud:
* reaktanter: Bly (ii) nitrat (Pb (NO₃) ₂) og kaliumiodid (KI) er begge vandige opløsninger (aq).
* Produkter: Bly (ii) iodid (PBI₂) er et gult fast bundfald (er), mens kaliumnitrat (Kno₃) forbliver i opløsning (aq).
Denne reaktion betragtes også som en nedbørreaktion Fordi dannelsen af den uopløselige bly (II) iodid får den til at udfælde ud af opløsningen.
Sidste artikelHvordan forårsager grundvand kemisk forvitring?
Næste artikelHvor mange mol sølvatomer er i 1,8 x 10 20 sølv?
 Varme artikler
Varme artikler
-
 Reparation af huller lavet miljøvenligt ved hjælp af grus fra spildevandsrensningForskere forvandler grus fra spildevand (til venstre) til en keramisk mørtel, der kan bruges som hulfyldningsmiddel (til højre). Kredit:Zhongzhe Liu Huller er skærpende at køre over, og de kan for
Reparation af huller lavet miljøvenligt ved hjælp af grus fra spildevandsrensningForskere forvandler grus fra spildevand (til venstre) til en keramisk mørtel, der kan bruges som hulfyldningsmiddel (til højre). Kredit:Zhongzhe Liu Huller er skærpende at køre over, og de kan for -
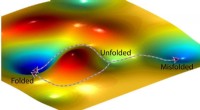 Skjult symmetri fundet i kemiske kinetiske ligningerEn kunstners repræsentation af et landskab med fri energi og to mulige veje, et protein kan følge (venstre) for at folde korrekt og en tredje vej (til højre), der fører til en fejlfoldet tilstand. Kre
Skjult symmetri fundet i kemiske kinetiske ligningerEn kunstners repræsentation af et landskab med fri energi og to mulige veje, et protein kan følge (venstre) for at folde korrekt og en tredje vej (til højre), der fører til en fejlfoldet tilstand. Kre -
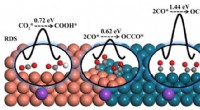 Tuning reaktionsbarrierer for kuldioxid elektroreduktion til multicarbon produkterEn intim CuPd(100)-grænseflade blev designet til at sænke energibarriererne for mellemreaktion (CO2*-hydrogenering og C-C-kobling) og forbedre effektiviteten af C2-produkter. Den optimale CuPd(100)-
Tuning reaktionsbarrierer for kuldioxid elektroreduktion til multicarbon produkterEn intim CuPd(100)-grænseflade blev designet til at sænke energibarriererne for mellemreaktion (CO2*-hydrogenering og C-C-kobling) og forbedre effektiviteten af C2-produkter. Den optimale CuPd(100)- -
 Redoxdivergerende strategi til konstruktion af (dihydro)thiophener med dimethylsulfoxidKredit:Pixabay/CC0 Public Domain (dihydro)thiophener, blandt de mest almindelige femleddede heterocykler, er udbredt i et stort antal naturlige produkter, funktionelle materialer, og biologisk akt
Redoxdivergerende strategi til konstruktion af (dihydro)thiophener med dimethylsulfoxidKredit:Pixabay/CC0 Public Domain (dihydro)thiophener, blandt de mest almindelige femleddede heterocykler, er udbredt i et stort antal naturlige produkter, funktionelle materialer, og biologisk akt
- Hvilken slags rock produceres, når sedimentær sandsten gennemgår metamorfisme?
- Forskere opdager den tidligste registrerede blyeksponering i 250, 000 år gamle neandertaler tænder
- Forskere ved MAJORANA Collaboration leder efter regelovertrædende elektroner
- Fossiler af sauropodomorfe forfader viser, at den gik oprejst, var hurtig og adræt
- Hvor meget fluor er for meget fluor?
- Betydningen af følelser:Kulturel og biologisk evolution påvirker, hvordan mennesker føler føle…


