Hvad vil danne kovalente bindinger med fluor?
Her er en sammenbrud af, hvad der vil danne kovalente bindinger med fluor:
bestemt:
* Andre halogener: Chlor (CL), brom (BR) og jod (I) vil alle danne kovalente bindinger med fluor.
* ilt (O): Formularer kovalente bindinger med fluor i forbindelser som iltdifluorid (af₂).
* nitrogen (n): Formularer kovalente bindinger med fluor i forbindelser som nitrogentrifluorid (NF₃).
* carbon (c): Formularer kovalente bindinger med fluor i forbindelser som tetrafluoroethylen (C₂f₄) og carbontetrafluorid (CF₄).
* brint (H): Danner en kovalent binding med fluor i brintfluorid (HF).
Mindre sandsynligt (men stadig muligt):
* Nogle mindre elektronegative ikke -metaller: Elementer som svovl (er), fosfor (P) og selen (SE) kan danne kovalente bindinger med fluor, men disse bindinger er ofte svagere og mindre stabile.
Hvad danner ikke kovalente bindinger med fluor:
* Metaller: Metaller har en tendens til at miste elektroner for at danne ioniske bindinger, ikke dele dem. Selvom der muligvis er nogle usædvanlige tilfælde, danner metaller generelt ikke kovalente bindinger med fluor.
Vigtig note: Elektronegativitetsforskellen mellem de to atomer kan påvirke den dannede bindingstype. Mens fluor let vil danne kovalente bindinger, kan meget store elektronegativitetsforskelle føre til polære kovalente bindinger eller endda ioniske bindinger.
Sidste artikelEr klor et metal ikke -meta eller metaloid?
Næste artikelHvad er et oxid af et overgangselement?
 Varme artikler
Varme artikler
-
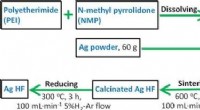 Forskere foreslår en ny metode til at forbedre den elektrokatalytiske omdannelse af kuldioxidDiagram over de detaljerede fremstillingsprocedurer for Ag HF. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202210432 Et forskerhold ledet af Profs. Chen Wei og Wei Wei f
Forskere foreslår en ny metode til at forbedre den elektrokatalytiske omdannelse af kuldioxidDiagram over de detaljerede fremstillingsprocedurer for Ag HF. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202210432 Et forskerhold ledet af Profs. Chen Wei og Wei Wei f -
 Forskere finder nye måder at bruge bioraffinaderikemikalier påSkræddersyede designerbakterier som fremtidige værktøjer i valoriseringen af bioraffinaderi-furaner. Kredit:Jan Deska Forskere fra gruppen Synthetic Organic Chemistry ved Aalto Universitet har e
Forskere finder nye måder at bruge bioraffinaderikemikalier påSkræddersyede designerbakterier som fremtidige værktøjer i valoriseringen af bioraffinaderi-furaner. Kredit:Jan Deska Forskere fra gruppen Synthetic Organic Chemistry ved Aalto Universitet har e -
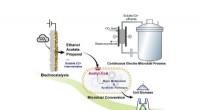 Teamet designer system til at skabe bioplastGrafisk abstrakt. Kredit:Chem (2022). DOI:10.1016/j.chempr.2022.09.005 Et team af Texas A&M AgriLife Research-forskere har udviklet et system, der bruger kuldioxid, CO2 , for at producere bionedbry
Teamet designer system til at skabe bioplastGrafisk abstrakt. Kredit:Chem (2022). DOI:10.1016/j.chempr.2022.09.005 Et team af Texas A&M AgriLife Research-forskere har udviklet et system, der bruger kuldioxid, CO2 , for at producere bionedbry -
 Præcise magneter 3-D printet af specielt rustfrit stålEmpa præcist magnetiseret:Jernspåner klæber til dette mini skakbræt med fire millimeter kantlængde. Den delvist magnetiske struktur blev fremstillet af en enkelt type stålkraft ved forskellige tempera
Præcise magneter 3-D printet af specielt rustfrit stålEmpa præcist magnetiseret:Jernspåner klæber til dette mini skakbræt med fire millimeter kantlængde. Den delvist magnetiske struktur blev fremstillet af en enkelt type stålkraft ved forskellige tempera
- Hvad er to måder vand konverteres til damp?
- Hvad er der nødvendigt for at erstatte elektrisk energi trukket fra batteriet?
- Hvorfor falder genstande, der er runde hurtigere end flade?
- Hvorfor har radiobølger mindst mulig energi alle elektromagnetiske bølgelængder?
- Hvordan ville en skabning se ud som at leve på Saturn planeten?
- Sådan fejlfindes enkeltfasemotorer


