Hvad er et oxid af et overgangselement?
Her er en sammenbrud:
* Overgangselementer: Dette er elementer placeret i D-blokken i den periodiske tabel, kendt for deres variable oxidationstilstande og evnen til at danne farverige forbindelser. Eksempler inkluderer jern (Fe), kobber (Cu), mangan (MN) og chrom (CR).
* Oxider: Oxider er kemiske forbindelser, der indeholder mindst et iltatom og et andet element.
Egenskaber ved overgangsmetaloxider:
* Variabel oxidation siger: Overgangsmetaller kan udvise flere oxidationstilstande, hvilket fører til en række oxider med forskellige kemiske formler og egenskaber. For eksempel kan jern danne FeO (jern (II) oxid), Fe2O3 (jern (III) oxid) og Fe3O4 (jern (II, III) oxid).
* farvede forbindelser: Mange overgangsmetaloxider er farverige på grund af tilstedeværelsen af D-elektroner, der kan absorbere og udsende specifikke bølgelængder af lys.
* forskellige applikationer: Overgangsmetaloxider har en bred vifte af applikationer, herunder:
* pigmenter: Jernoxider bruges som pigmenter i maling, keramik og kosmetik.
* katalysatorer: Nogle oxider, som mangandioxid (MNO2), bruges som katalysatorer i forskellige kemiske reaktioner.
* Elektronik: Oxider som titandioxid (TiO2) anvendes i solceller og elektroniske anordninger.
Eksempler på overgangsmetaloxider:
* jernoxid (FEO) :Sort fast stof, brugt i pigmenter og stålfremstilling.
* kobberoxid (CUO) :Sort fast stof, brugt som katalysator og i keramik.
* manganoxid (MNO2) :Brunt fast stof, brugt som katalysator og i batterier.
* kromoxid (CR2O3) :Grønt fast stof, brugt som et pigment og i belægninger.
Sammenfattende er oxider af overgangselementer en forskelligartet gruppe af forbindelser med unikke egenskaber og vigtige anvendelser. Deres variable oxidationstilstande og farverige natur gør dem til fascinerende studiepersoner inden for kemi.
 Varme artikler
Varme artikler
-
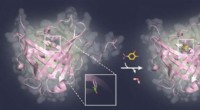 Blokering af sukkerstrukturer på vira og tumorcellerProf. Skerras aktuelle forskningsresultater baner vejen for udviklingen af nye typer bindingsproteiner til biologiske sukkerstrukturer, som spiller en væsentlig rolle ved kræft såvel som infektionss
Blokering af sukkerstrukturer på vira og tumorcellerProf. Skerras aktuelle forskningsresultater baner vejen for udviklingen af nye typer bindingsproteiner til biologiske sukkerstrukturer, som spiller en væsentlig rolle ved kræft såvel som infektionss -
 Brændselscelle røntgenundersøgelse beskriver virkningerne af temperatur og fugt på ydeevnenEn røntgenundersøgelse afslørede størrelsen og fordelingen af bittesmå lommer af vand i fibrøse brændstofcellekomponenter ved forskellige temperaturer. Kredit:Berkeley Lab Som en velplejet drivh
Brændselscelle røntgenundersøgelse beskriver virkningerne af temperatur og fugt på ydeevnenEn røntgenundersøgelse afslørede størrelsen og fordelingen af bittesmå lommer af vand i fibrøse brændstofcellekomponenter ved forskellige temperaturer. Kredit:Berkeley Lab Som en velplejet drivh -
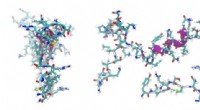 Cellulært stressforsvarKredit:CC0 Public Domain Små varmechokproteiner (sHSPer) er molekylære chaperoner, der binder til udfoldede proteiner for at forhindre proteinaggregering og forsvare mod cellulær stress. Mutatione
Cellulært stressforsvarKredit:CC0 Public Domain Små varmechokproteiner (sHSPer) er molekylære chaperoner, der binder til udfoldede proteiner for at forhindre proteinaggregering og forsvare mod cellulær stress. Mutatione -
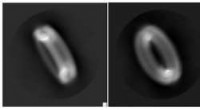 Guardians of the Ring—Forskere afslører strukturen af protein involveret i inflammatoriske sygdom…Cryo-EM-teknologi fangede elegante detaljer i gasdermin-poren. Kredit:Wu lab Når kroppen opdager en trussel, det være sig en viral invader eller en Alzheimers sygdom plaque, guardian proteiner på
Guardians of the Ring—Forskere afslører strukturen af protein involveret i inflammatoriske sygdom…Cryo-EM-teknologi fangede elegante detaljer i gasdermin-poren. Kredit:Wu lab Når kroppen opdager en trussel, det være sig en viral invader eller en Alzheimers sygdom plaque, guardian proteiner på
- Når H2S brænder, konverteres det, i hvilken gas?
- Hvad er de grundstoffer, der udgør magnesiumstearat?
- Myten om, hvordan videnskaben skrider frem, er bygget på en fejllæsning af historien om penicillin
- Rapport:Moratorium for udsættelse under COVID-19 beskytter udsatte børn
- Hvad er højden af lavest flyvende satellit?
- Ny forskning undersøger erfaringer fra raciserede samfund under COVID-19


