Hvad er gruppen af alkaliske jordmetaller?
Her er elementerne i denne gruppe:
* beryllium (BE)
* magnesium (mg)
* calcium (CA)
* strontium (SR)
* barium (BA)
* radium (RA)
Disse elementer deler flere nøgleegenskaber:
* de er alle metaller.
* de har to valenselektroner (elektroner i deres yderste skal). Dette betyder, at de har en tendens til at miste disse to elektroner til dannelse af +2 ioner, hvilket gør dem meget reaktive.
* de er sølvfarvede i farve, skønt de kan plette hurtigt.
* de er relativt bløde, men hårdere end alkalimetaller.
* de er gode ledere af elektricitet og varme.
* de reagerer let med vand for at danne alkaliske opløsninger.
Bemærk: Radium er radioaktivt og ikke så almindeligt som de andre medlemmer af gruppen.
Sidste artikelEr densitet en fysisk eller kemisk egenskab?
Næste artikelHvorfor har kaliumchlorid et højt smeltepunkt?
 Varme artikler
Varme artikler
-
 Anti-aging protein alpha Klothos molekylær struktur afsløretUT sydvestlige forskere har hjulpet med at afsløre den molekylære struktur af alfa Klotho (a-Klotho), det såkaldte “anti-aging” protein. Kredit:UT Southwestern Medical Center Forskere fra UT South
Anti-aging protein alpha Klothos molekylær struktur afsløretUT sydvestlige forskere har hjulpet med at afsløre den molekylære struktur af alfa Klotho (a-Klotho), det såkaldte “anti-aging” protein. Kredit:UT Southwestern Medical Center Forskere fra UT South -
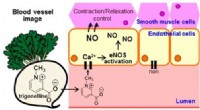 Forbindelser i monsterræddike kunne hjælpe med at tæmme hjerte-kar-sygdommeKredit:American Chemical Society Træd gulerødder til side, løg og broccoli. Den nyeste hjertesunde grøntsag kunne være en gigantisk, rekordsættende radise. I en undersøgelse, der vises i ACS Tids
Forbindelser i monsterræddike kunne hjælpe med at tæmme hjerte-kar-sygdommeKredit:American Chemical Society Træd gulerødder til side, løg og broccoli. Den nyeste hjertesunde grøntsag kunne være en gigantisk, rekordsættende radise. I en undersøgelse, der vises i ACS Tids -
 Beregningsmetode øger designeffektiviteten af proteinbaserede lægemidlerKredit:CC0 Public Domain Forskere fra Institut for Bioteknologi og Biomedicin (IBB), i samarbejde med forskere fra universitetet i Warszawa for nylig præsenteret en vigtig opdatering af deres AGGR
Beregningsmetode øger designeffektiviteten af proteinbaserede lægemidlerKredit:CC0 Public Domain Forskere fra Institut for Bioteknologi og Biomedicin (IBB), i samarbejde med forskere fra universitetet i Warszawa for nylig præsenteret en vigtig opdatering af deres AGGR -
 Forskning ser på materialets friktionsegenskaberSandia National Laboratories forskere Michael Chandross, venstre, og Nicolas Argibay viser en computersimulering og et ultrahøjt vakuum tribometer brugt til friktions- og slidtest, som er blandt de væ
Forskning ser på materialets friktionsegenskaberSandia National Laboratories forskere Michael Chandross, venstre, og Nicolas Argibay viser en computersimulering og et ultrahøjt vakuum tribometer brugt til friktions- og slidtest, som er blandt de væ
- Hvorfor vibrerer mus, når du henter dem?
- Succesfulde byparker får forskellige samfund til at føle sig trygge og velkomne - denne Minnesota-…
- Forskerhold løser årtier lange problem inden for mikroskopi
- Hvad kaldes en stejl bakke undertiden?
- Hvordan COVID har ændret den måde, amerikanere arbejder på, og hvor mange penge de har
- Hvad sker der, når to bevægelige genstande kolliderer, men den ene går hurtigere end den anden?


