Skriv den kemiske formel for en forbindelse, der har et calciumatom, og 2 kloratomer forudsiger binding mellem dem?
Her er hvorfor:
* calcium (CA) er i gruppe 2 i den periodiske tabel, hvilket betyder, at den har 2 valenselektroner (elektroner i dets yderste skal). Det har en tendens til at miste disse 2 elektroner for at opnå en stabil elektronkonfiguration.
* klor (Cl) er i gruppe 17 i den periodiske tabel, hvilket betyder, at den har 7 valenselektroner. Det har en tendens til at få en elektron for at opnå en stabil elektronkonfiguration.
For at danne en stabil forbindelse mister et calciumatom sine to valenselektroner, og to chloratomer får hver en elektron. Dette resulterer i:
* Calcium danner en +2 ion (Ca²⁺)
* Chlor danner to -1 ioner (2Cl⁻)
Gebyrerne afbalanceres, danner forbindelsen cacl₂ .
Bindingen mellem calcium og klor er en ionisk binding. Dette skyldes, at det ene atom (calcium) mister elektroner for at blive positivt ladet, mens det andet atom (klor) får elektroner til at blive negativt ladet. De modsatte afgifter tiltrækker hinanden og danner en stærk elektrostatisk attraktion kendt som en ionisk binding.
 Varme artikler
Varme artikler
-
 Forskere opfinder en ny måde at skabe kødanaloger påKredit:Immanuel Kant Baltic Federal University Verdensomspændende fokus på kødanaloger bliver ved med at stige for at begynde at producere vegetabilske proteinprodukter uden kolesterol, der indeho
Forskere opfinder en ny måde at skabe kødanaloger påKredit:Immanuel Kant Baltic Federal University Verdensomspændende fokus på kødanaloger bliver ved med at stige for at begynde at producere vegetabilske proteinprodukter uden kolesterol, der indeho -
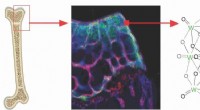 Musestudie giver indsigt i, hvordan metallet akkumuleres i knoglevævHos mus udsat for wolfram i drikkevand, elementet akkumuleret i porøst væv nær enden af knogler (til venstre). Ved hjælp af synkrotronbaserede røntgenabsorptionsteknikker, forskere fremstillede et b
Musestudie giver indsigt i, hvordan metallet akkumuleres i knoglevævHos mus udsat for wolfram i drikkevand, elementet akkumuleret i porøst væv nær enden af knogler (til venstre). Ved hjælp af synkrotronbaserede røntgenabsorptionsteknikker, forskere fremstillede et b -
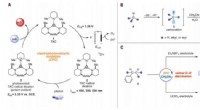 Elektrofotokatalytisk diamination af vicinale C -H -bindingerElektrofotokatalytisk amination af C -H -bindinger. (A) Generisk elektrofotokatalytisk cyklus med trisaminocyclopropenium (TAC) 1. (B) Ritter-type C-H amineringsreaktion. (C) Elektrofotokatalytiske vi
Elektrofotokatalytisk diamination af vicinale C -H -bindingerElektrofotokatalytisk amination af C -H -bindinger. (A) Generisk elektrofotokatalytisk cyklus med trisaminocyclopropenium (TAC) 1. (B) Ritter-type C-H amineringsreaktion. (C) Elektrofotokatalytiske vi -
 Undersøgelse af nitrogen-doterede polycykliske aromatiske kulbrinter til højtydende OLED'erInden for de nye OLEDer lyser forskerne selv det mørkeste mørke op. Billedet er taget af Neonmuseet i Warszawa. Kredit:Kilde IPC PAS, Grzegorz Krzyzewski Elektroniske visuelle skærme er kommet lang
Undersøgelse af nitrogen-doterede polycykliske aromatiske kulbrinter til højtydende OLED'erInden for de nye OLEDer lyser forskerne selv det mørkeste mørke op. Billedet er taget af Neonmuseet i Warszawa. Kredit:Kilde IPC PAS, Grzegorz Krzyzewski Elektroniske visuelle skærme er kommet lang


