Hvor mange mol Cl -ioner er der behov for for at kombinere fuldstændigt med 0,25 mg 2 ioner?
1. Bestem den kemiske formel:
* Magnesium (Mg) har en +2 ladning (mg²⁺).
* Chlor (CL) har en -1 -ladning (CL⁻).
For at afbalancere ladningerne har vi brug for to chloridioner for hver magnesiumion. Den kemiske formel for forbindelsen er mgcl₂ (magnesiumchlorid).
2. Molforhold:
* Formlen MgCl₂ fortæller os, at 1 mol mg²⁺ -ioner kombineres med 2 mol Cl⁻ioner.
3. Beregn mol af Cl⁻:
* Da vi har 0,25 mol mg²⁺ -ioner, har vi brug for det dobbelte af den mængde Cl⁻ioner.
* Mol Cl⁻ =0,25 mol mg²⁺ * (2 mol cl⁻ / 1 mol mg²⁺) = 0,50 mol cl⁻
Derfor er der behov for 0,50 mol Cl⁻ioner for at kombinere fuldstændigt med 0,25 mol mg²⁺ioner.
 Varme artikler
Varme artikler
-
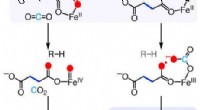 Vejen til fremstilling af ethylenMekanismer for de ethylen-dannende enzym (EFE) reaktioner. Ny forskning beskriver de kemiske trin, som dette naturligt forekommende enzym bruger til at omdanne en almindelig kemisk forbindelse til eth
Vejen til fremstilling af ethylenMekanismer for de ethylen-dannende enzym (EFE) reaktioner. Ny forskning beskriver de kemiske trin, som dette naturligt forekommende enzym bruger til at omdanne en almindelig kemisk forbindelse til eth -
 Teknologier til enkeltcellet RNA-profilering kan hjælpe med at dissekere de cellulære baser af kom…Alex K. Shalek, en MIT-lektor i kemi, bruger teknologier såsom enkeltcellet RNA-sekventering til at analysere forskelle i genekspressionsmønstre for individuelle celler og til at finde ud af, hvordan
Teknologier til enkeltcellet RNA-profilering kan hjælpe med at dissekere de cellulære baser af kom…Alex K. Shalek, en MIT-lektor i kemi, bruger teknologier såsom enkeltcellet RNA-sekventering til at analysere forskelle i genekspressionsmønstre for individuelle celler og til at finde ud af, hvordan -
 Simuleringer viser, hvordan beta-amyloid kan dræbe neurale cellerGanesan Narsimhan (til højre) og Xiao Zhu simulerede den effekt beta-amyloid peptider har på neurale celler, viser, hvilken rolle disse stoffer kan have i at forårsage hjernecelledød og nogle neurodeg
Simuleringer viser, hvordan beta-amyloid kan dræbe neurale cellerGanesan Narsimhan (til højre) og Xiao Zhu simulerede den effekt beta-amyloid peptider har på neurale celler, viser, hvilken rolle disse stoffer kan have i at forårsage hjernecelledød og nogle neurodeg -
 Forskere afdækker skjulte deicer -risici, der påvirker broens sundhedXianming Shi. Kredit:WSU Almindelige magnesiumchlorid tømidler, der bruges på veje og broer rundt om i USA, kan gøre mere skade end tidligere antaget, forskere har fundet. Derudover at skade er u
Forskere afdækker skjulte deicer -risici, der påvirker broens sundhedXianming Shi. Kredit:WSU Almindelige magnesiumchlorid tømidler, der bruges på veje og broer rundt om i USA, kan gøre mere skade end tidligere antaget, forskere har fundet. Derudover at skade er u
- Når natrium og klorbinding, hvilken slags er dette?
- Hvad gør høj energi i et instrument?
- Hvordan tusindårig nostalgi gav næring til succesen med 'Pokemon Go'
- Et pust af ingenting giver et nyt perspektiv på superledning
- Forskere måler med succes nogle af elektronernes kvanteegenskaber i 2-D halvledere
- Hvad gør mosekroppe anderledes end ørkenmumier?


