Hvad laver brint og kulstof?
Hvorfor så mange forbindelser?
* alsidig binding: Carbon har fire valenselektroner, hvilket giver det mulighed for at danne fire bindinger med andre atomer, inklusive brint. Dette giver kulstof en bemærkelsesværdig evne til at skabe lange kæder og komplekse strukturer.
* kulbrinter: De enkleste forbindelser lavet af kun brint og kulstof kaldes kulbrinter. De danner grundlaget for mange organiske molekyler.
Eksempler på forbindelser:
* methan (CH4): Det enkleste carbonhydrid, en vigtig komponent i naturgas.
* ethan (C2H6): Et andet simpelt carbonhydrid, der også findes i naturgas.
* propan (C3H8): Et almindeligt brændstof til madlavning og opvarmning.
* butan (C4H10): Fundet i lettere væske og nogle brændstofkilder.
* ethylen (C2H4): En afgørende byggesten til plast og andre industrielle kemikalier.
* benzen (C6H6): En grundlæggende forbindelse til mange farmaceutiske stoffer og andre organiske kemikalier.
* polymerer: Lange kæder med gentagne enheder, herunder plast som polyethylen (fremstillet af ethylen).
ud over kulbrinter:
Tilsætning af andre elementer som ilt, nitrogen og svovl til blandingen skaber endnu mere forskellige forbindelser. Disse inkluderer:
* Alkoholer: Indeholder en hydroxylgruppe (-OH) som ethanol (drikke alkohol).
* aldehyder &ketoner: Har en carbonylgruppe (C =O) som acetone (neglelakfjerner).
* carboxylsyrer: Indeholder en carboxylgruppe (-cooh) som eddikesyre (eddike).
* aminer: Indeholder nitrogen som methylamin (brugt i gødningsproduktion).
Konklusion:
Kombinationen af brint og kulstof giver grundlaget for en utrolig enorm og forskelligartet række forbindelser, der er essentielt for vores hverdag og selve livets kemi.
Sidste artikelHvorfor reagerer en vandig opløsning af jod ikke med natriumbromid?
Næste artikelHvad er den kemiske formel for fosfat?
 Varme artikler
Varme artikler
-
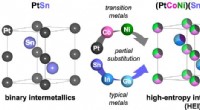 Carbonneutraliserende propylenproduktion katalyserer ændringer i petrokemisk teknikPlatin (Pt) og tin (Sn) steder i intermetallisk PtSn er delvist substitueret med henholdsvis Cobalt og nikkel (Co/Ni) og Indium og Gallium (In/Ga), hvilket danner en PtSn-type højentropi intermetallis
Carbonneutraliserende propylenproduktion katalyserer ændringer i petrokemisk teknikPlatin (Pt) og tin (Sn) steder i intermetallisk PtSn er delvist substitueret med henholdsvis Cobalt og nikkel (Co/Ni) og Indium og Gallium (In/Ga), hvilket danner en PtSn-type højentropi intermetallis -
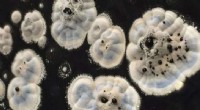 Hvor gamle forbindelser kunne blive morgendagens livreddereKredit:University of Leeds University of Leeds forskere ser tilbage i tiden på tidligere kasserede kemiske forbindelser, for at se, om der kunne udvikles nogen til nye antibiotika. I antibiotikau
Hvor gamle forbindelser kunne blive morgendagens livreddereKredit:University of Leeds University of Leeds forskere ser tilbage i tiden på tidligere kasserede kemiske forbindelser, for at se, om der kunne udvikles nogen til nye antibiotika. I antibiotikau -
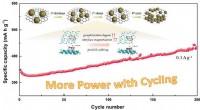 Partikelforfining inducerer og øger cykluskapaciteten af natrium/lithium-ion-batterierSkematisk diagram af mekanismen for partikelforfining for at inducere forøgelse af cykluskapaciteten af SIBer. Kredit:WANG Canpei Natriumionbatterier (SIBer) har tiltrukket bred opmærksomhed på
Partikelforfining inducerer og øger cykluskapaciteten af natrium/lithium-ion-batterierSkematisk diagram af mekanismen for partikelforfining for at inducere forøgelse af cykluskapaciteten af SIBer. Kredit:WANG Canpei Natriumionbatterier (SIBer) har tiltrukket bred opmærksomhed på -
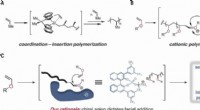 Brug af en organokatalysator til at stereokontrollere polymerisationDesign af en stereoselektiv kationisk polymerisation. (A) Det chirale ligandmiljø i koordinations-insertion-polymerisationer muliggør stereoselektiv monomer-enchainment ved at dirigere ansigtsaddition
Brug af en organokatalysator til at stereokontrollere polymerisationDesign af en stereoselektiv kationisk polymerisation. (A) Det chirale ligandmiljø i koordinations-insertion-polymerisationer muliggør stereoselektiv monomer-enchainment ved at dirigere ansigtsaddition
- Supercomputere kaster nyt lys over havturbulens
- Hvad er de indre kerner af tråd lavet, og hvorfor?
- Hvilke af disse sonder var den første omfattende kortoverflademåne?
- Startups tackler indiske kvinders toiletproblemer
- Hvad forårsager sværmende myrer?
- Kollektiv kvanteeffekt:Når elektroner holder sammen


