Er siliciumchlorid en polær binding?
* polære obligationer: Silicium (SI) er mindre elektronegativ end klor (CL). Dette betyder, at klor tiltrækker de delte elektroner i SI-CL-bindingen stærkere, hvilket skaber en delvis negativ ladning på chloratomet og en delvis positiv ladning på siliciumatomet. Denne ujævne deling af elektroner gør SI-CL Bond Polar.
* ikke -polært molekyle: Selvom SICL₄ har polære bindinger, resulterer molekylets tetrahedrale form i de individuelle bindingsdipoler, der annullerer hinanden. Tænk på det som en trækkraft, hvor alle holdene trækker med lige kraft i forskellige retninger-ingen vinder! Dette symmetriske arrangement fører til et netto dipolmoment på nul, hvilket gør molekylet ikke -polært.
Sidste artikelHvorfor tilsætte svovlsyre i sulfateret aske?
Næste artikelSkift fra flydende vand til damp?
 Varme artikler
Varme artikler
-
 Ioniske edderkoppespind, der imiterer dobbelte funktioner i ægte edderkoppespindKredit:Unsplash/CC0 Public Domain Et team af forskere fra Seoul National University og Eumam Middle School har udviklet en type ionisk edderkoppespind, der er i stand til at efterligne dobbelte fu
Ioniske edderkoppespind, der imiterer dobbelte funktioner i ægte edderkoppespindKredit:Unsplash/CC0 Public Domain Et team af forskere fra Seoul National University og Eumam Middle School har udviklet en type ionisk edderkoppespind, der er i stand til at efterligne dobbelte fu -
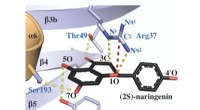 Nøgleenzym fundet i planter kan styre udviklingen af medicin og andre produkterProtein røntgenkrystalstrukturen af chalcone isomerase, kompleksbundet med et produktmolekyle kaldet (2S)-naringenin, afslører, hvordan det aktive sted arginin (mærket som Arg 37) letter katalyse af
Nøgleenzym fundet i planter kan styre udviklingen af medicin og andre produkterProtein røntgenkrystalstrukturen af chalcone isomerase, kompleksbundet med et produktmolekyle kaldet (2S)-naringenin, afslører, hvordan det aktive sted arginin (mærket som Arg 37) letter katalyse af -
 Cryo-EM afslører interaktion mellem store lægemiddelmålGPCR-Gi struktur. Kredit:Xu Laboratory, Van Andel Research Institute For første gang, forskere har visualiseret interaktionen mellem to kritiske komponenter i kroppens enorme cellulære kommunikati
Cryo-EM afslører interaktion mellem store lægemiddelmålGPCR-Gi struktur. Kredit:Xu Laboratory, Van Andel Research Institute For første gang, forskere har visualiseret interaktionen mellem to kritiske komponenter i kroppens enorme cellulære kommunikati -
 Studerer gasmaskefiltre, så folk kan trække vejret lettereKobber, vist her, er en komponent i filtre, der bruges i gasmasker for at beskytte brugere mod giftige kemikalier. Forskere ved Berkeley Lab bruger kraftig røntgenspektroskopi til at studere de moleky
Studerer gasmaskefiltre, så folk kan trække vejret lettereKobber, vist her, er en komponent i filtre, der bruges i gasmasker for at beskytte brugere mod giftige kemikalier. Forskere ved Berkeley Lab bruger kraftig røntgenspektroskopi til at studere de moleky
- Deadlines kan være effektive til at opbygge støtte til klimaændringsforanstaltninger
- Jorden i sin bane, der bevæger sig tættere på solen, forårsager hvad i alverden?
- Tredimensionelle punktskyer giver indsigt i skovenes strukturelle kompleksitet
- Nyt AI-værktøj identificerer kræftudfald ved hjælp af radiologirapporter
- Forskere skal udføre en stor undersøgelse af mikroplastik i det japanske hav
- Video:Olivenolies kemi


