2 Forudsig og forklar, hvilke systemer der elektrisk udfører en solid NaCl B smeltet C En vandig opløsning af NaCl?
solid NaCl (bordsalt)
* Konduktivitet: Ikke-ledende
* Forklaring: I faste NaCl er natrium (Na+) og chlorid (Cl-) -ioner arrangeret i en tæt pakket, krystallinsk gitter. Disse ioner er fastgjort i deres positioner og kan ikke bevæge sig frit. Mens ionerne har en ladning, forhindrer deres immobilitet strømmen af elektricitet.
smeltet NaCl
* Konduktivitet: Dirigere
* Forklaring: Når NaCl er smeltet, går de ioniske bindinger, der holder gitteret sammen. Dette gør det muligt for Na+ og kloderne at bevæge sig frit gennem væsken. Nu hvor de ladede partikler kan bevæge sig, kan de bære en elektrisk strøm.
vandig løsning af NaCl
* Konduktivitet: Dirigere
* Forklaring: Når NaCl opløses i vand, adskiller den sig til Na+ og Cl- ioner. Disse ioner bliver omgivet af vandmolekyler (hydrering), hvilket giver dem mulighed for at bevæge sig frit gennem opløsningen. Denne mobilitet af ladede partikler gør opløsningen elektrisk ledende.
Kortfattet:
* fast: Ioner er faste, ingen fri bevægelighed, ingen ledningsevne.
* smeltet: Ioner er fri til at bevæge sig, ledningsevnen er til stede.
* vandig: Ioner er fri til at bevæge sig i opløsning, ledningsevne er til stede.
Sidste artikelVille brom og ilt danne en ionisk forbindelse?
Næste artikelHvad angiver et sammensat element?
 Varme artikler
Varme artikler
-
 Blokering af sukkerstrukturer på vira og tumorcellerProf. Skerras aktuelle forskningsresultater baner vejen for udviklingen af nye typer bindingsproteiner til biologiske sukkerstrukturer, som spiller en væsentlig rolle ved kræft såvel som infektionss
Blokering af sukkerstrukturer på vira og tumorcellerProf. Skerras aktuelle forskningsresultater baner vejen for udviklingen af nye typer bindingsproteiner til biologiske sukkerstrukturer, som spiller en væsentlig rolle ved kræft såvel som infektionss -
 Bæredygtig vandkvalitetssensor lavet af menneskehår-afledte kulstofprikkerKredit:CC0 Public Domain Griffith University-forskere har brugt menneskehåraffald til at udvikle bæredygtige organiske højteknologiske enheder til vandkvalitetstest af forurenende stoffer. Profes
Bæredygtig vandkvalitetssensor lavet af menneskehår-afledte kulstofprikkerKredit:CC0 Public Domain Griffith University-forskere har brugt menneskehåraffald til at udvikle bæredygtige organiske højteknologiske enheder til vandkvalitetstest af forurenende stoffer. Profes -
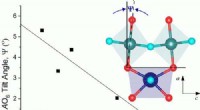 Opbygning af viden om ændringer i urankemiKredit:Australian Nuclear Science and Technology Organisation (ANSTO) Der er stadig rigtig mange spørgsmål, der skal besvares inden for urankemi, især i forbindelse med det nukleare brændselskreds
Opbygning af viden om ændringer i urankemiKredit:Australian Nuclear Science and Technology Organisation (ANSTO) Der er stadig rigtig mange spørgsmål, der skal besvares inden for urankemi, især i forbindelse med det nukleare brændselskreds -
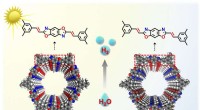 Nye isomere vinylen-bundne kovalente organiske rammer udviklet med distinkte fotokatalytiske egenska…De isomere vinylen-bundne kovalente organiske rammer. Kredit:NIMTE Forskere ledet af prof. Zahng Tao ved Ningbo Institute of Materials Technology and Engineering (NIMTE) fra det kinesiske videnskab
Nye isomere vinylen-bundne kovalente organiske rammer udviklet med distinkte fotokatalytiske egenska…De isomere vinylen-bundne kovalente organiske rammer. Kredit:NIMTE Forskere ledet af prof. Zahng Tao ved Ningbo Institute of Materials Technology and Engineering (NIMTE) fra det kinesiske videnskab
- Hvordan byvarme påvirker bibestanden
- Hubble udsigt over kosmiske støvbaner
- Airbus irriteret over Spaniens valg af kampflypartner
- Hvad hedder den magt, der også kunne bremse Donw Ball og dens bevægelse?
- Hvordan er sukker- og vandmolekyler ens?
- Voyager 2 kan ikke modtage kommandoer under NASAs 70 meter brede radioantenneopgraderinger


