Når kobbervendinger tilsættes til sølvnitratopløsning, hvorfor bliver det blå i farve?
Den kemiske reaktion
Denne reaktion er et klassisk eksempel på en enkelt forskydningsreaktion. Kobber (Cu) er mere reaktiv end sølv (Ag), så det fortrænger sølv fra sølvnitratopløsningen. Reaktionen ser sådan ud:
cu (s) + 2agno₃ (aq) → cu (no₃) ₂ (aq) + 2ag (s)
Forklaring
* kobber (cu) :Kobbervendingerne fungerer som reaktanten og giver kobberatomer, der vil være involveret i reaktionen.
* sølvnitrat (Agno₃) :Dette er det opløste salt i opløsning, hvilket giver de sølvioner (AG⁺), der er nødvendige til reaktionen.
* kobber (II) nitrat (Cu (no₃) ₂) :Når kobber reagerer med sølvnitrat, danner det kobber (II) nitrat, der opløses i opløsningen og er ansvarlig for den blå farve.
* sølv (AG) :Sølvioner fra opløsningen reduceres til massivt sølvmetal, der danner et gråt-hvidt bundfald i bunden af beholderen.
den blå farve
Den blå farve kommer fra dannelsen af kobber (II) -ioner (Cu²⁺) i opløsning. Kobber (ii) ioner har en karakteristisk blå farve, når de opløses i vand.
Kortfattet
1. Kobbervendingerne reagerer med sølvnitratopløsningen.
2. Kobber fortrænger sølv fra opløsningen og danner kobber (II) nitrat.
3. kobber (II) nitrat opløses i vand og producerer kobber (II) -ioner, som er blå.
4. den blå farve på kobber (II) -ionerne får opløsningen til at virke blå.
Sidste artikelMennesker ændrer jordens termostat til hvilken forbindelse?
Næste artikelHvilke elementer er i tinoxid?
 Varme artikler
Varme artikler
-
 Brint:fremtidens brændstof?Da løbet om at finde energikilder til at erstatte vores faldende fossile brændstofforsyninger fortsætter i hast, brint vil sandsynligvis spille en afgørende rolle i fremtiden. Kredit:Materials Researc
Brint:fremtidens brændstof?Da løbet om at finde energikilder til at erstatte vores faldende fossile brændstofforsyninger fortsætter i hast, brint vil sandsynligvis spille en afgørende rolle i fremtiden. Kredit:Materials Researc -
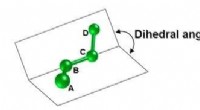 Fujitsu udvikler molekylær simuleringsteknologi til effektivt at skabe nye lægemiddelkandidaterFigur 1:Dihedral vinkel (vinklen dannet af planet skabt af atomer A, B, og C, og flyet skabt af atomer B, C, og D). Kredit:Fujitsu Fujitsu Laboratories annoncerede i dag udviklingen af molekylær
Fujitsu udvikler molekylær simuleringsteknologi til effektivt at skabe nye lægemiddelkandidaterFigur 1:Dihedral vinkel (vinklen dannet af planet skabt af atomer A, B, og C, og flyet skabt af atomer B, C, og D). Kredit:Fujitsu Fujitsu Laboratories annoncerede i dag udviklingen af molekylær -
 En ubrydelig kombination af usynlig blæk og kunstig intelligensMed almindelig blæk, en computer trænet med kodebogen afkoder STOP (øverst); når der vises et UV-lys på papiret, det usynlige blæk er blotlagt, og det rigtige budskab afsløres som BEGIN (nederst). Kre
En ubrydelig kombination af usynlig blæk og kunstig intelligensMed almindelig blæk, en computer trænet med kodebogen afkoder STOP (øverst); når der vises et UV-lys på papiret, det usynlige blæk er blotlagt, og det rigtige budskab afsløres som BEGIN (nederst). Kre -
 Fremstilling af fejlfrie metalkrystaller af en hidtil uset størrelse(A) Skematisk af kvartsholderen, som kobber (Cu) folien er suspenderet fra, (B) fotografi af konfigurationen vist skematisk i (A). (C) Fotografi af den glødede enkeltkrystal Cu -folie (ca. 2 cm × 8 cm
Fremstilling af fejlfrie metalkrystaller af en hidtil uset størrelse(A) Skematisk af kvartsholderen, som kobber (Cu) folien er suspenderet fra, (B) fotografi af konfigurationen vist skematisk i (A). (C) Fotografi af den glødede enkeltkrystal Cu -folie (ca. 2 cm × 8 cm
- Hvor blev jadeit fundet i USA?
- Undervandskulturarv:Studerer forældreløse genstande for at finde ud af, hvilke skibsvrag de kom fr…
- SpaceX administrerer endelig Kennedy Space Center-lanceringen med rekordbindingsbooster
- Undersøgelse undersøger rollen som dybhavsmikrobielle rovdyr ved hydrotermiske ventilationsåbning…
- Hvad er overfladearealet af salt?
- Undersøgelse viser, at plantehydraulik skaber streaming elektrisk potentiale synkroniseret med biol…


