Hvor mange kovalente bindinger dannes af silicium?
Her er hvorfor:
* Elektronkonfiguration: Silicon har en elektronkonfiguration af [NE] 3S² 3p². Det har fire elektroner i sin ydre skal, som er valensskallen.
* octet regel: For at opnå en stabil elektronkonfiguration (som de ædle gasser) skal silicium få fire flere elektroner. Det gør dette ved at dele sine fire valenselektroner med andre atomer og danne fire kovalente bindinger.
* Eksempel: I siliciumdioxid (SIO₂) danner hvert siliciumatom fire kovalente bindinger med to iltatomer.
 Varme artikler
Varme artikler
-
 På linjen:At se nanopartikler komme i formKredit:Lawrence Berkeley National Laboratory Flydende strukturer - flydende dråber, der bevarer en bestemt form - er nyttige til en række forskellige anvendelser, fra fødevareforarbejdning til kos
På linjen:At se nanopartikler komme i formKredit:Lawrence Berkeley National Laboratory Flydende strukturer - flydende dråber, der bevarer en bestemt form - er nyttige til en række forskellige anvendelser, fra fødevareforarbejdning til kos -
 Grønnere molekylære mellemprodukter kan hjælpe lægemiddeldesignLászló Kürti er på billedet. Kredit:Jeff Fitlow/Rice University Forskere ved Rice University har forenklet deres tilgang til at syntetisere en meget alsidig familie af prækursorer på vej til biolo
Grønnere molekylære mellemprodukter kan hjælpe lægemiddeldesignLászló Kürti er på billedet. Kredit:Jeff Fitlow/Rice University Forskere ved Rice University har forenklet deres tilgang til at syntetisere en meget alsidig familie af prækursorer på vej til biolo -
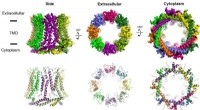 Nyt kig på mærkelige huller involveret i smag, Alzheimers, astmaVed hjælp af kryo-elektronmikroskopi, Furukawas laboratorium kompilerede et 3D-billede, der beskriver det nøjagtige arrangement af proteinerne, der former hver CALHM-pore. På billedet:CALHM1 set fra s
Nyt kig på mærkelige huller involveret i smag, Alzheimers, astmaVed hjælp af kryo-elektronmikroskopi, Furukawas laboratorium kompilerede et 3D-billede, der beskriver det nøjagtige arrangement af proteinerne, der former hver CALHM-pore. På billedet:CALHM1 set fra s -
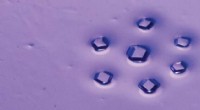 Låste MOF'er er nøglen til høj porøsitetMetal organiske rammer (MOFer) er krystallinske materialer fremstillet af metalioner forbundet med organiske linkere. De er ideelle til at være vært for forskellige molekyler og har fundet anvendelser
Låste MOF'er er nøglen til høj porøsitetMetal organiske rammer (MOFer) er krystallinske materialer fremstillet af metalioner forbundet med organiske linkere. De er ideelle til at være vært for forskellige molekyler og har fundet anvendelser
- Hvad er elektronkonfigurationen af CCL4?
- Egenskaber og anvendelser til 8620 Grade Steel
- Hvad er fordelen ved kilden til sol?
- Multiparty entanglement:Når alt er forbundet
- Forskere bygger nanoskala roterende apparater ved hjælp af tætsiddende 3D DNA-komponenter (m/ vide…
- Hvordan skabes energi ved hjælp af geotermisk?


