Hvor mange atomer er der i 55,8 gram FE?
1. Find den molære masse af jern:
* Den molære jernmasse er 55,845 g/mol (du kan finde dette på den periodiske tabel).
2. Beregn antallet af mol jern:
* Mol =masse / molær masse
* Mol =55,8 g / 55,845 g / mol
* Mol ≈ 1 mol
3. Brug Avogadros nummer for at finde antallet af atomer:
* Avogadros nummer er 6,022 x 10^23 atomer/mol.
* Antal atomer =mol X Avogadros nummer
* Antal atomer ≈ 1 mol x 6,022 x 10^23 atomer/mol
* Antal atomer ≈ 6,022 x 10^23 atomer
Derfor er der ca. 6,022 x 10^23 atomer i 55,8 gram jern.
Sidste artikelHvad består kun af kulstofhydrogen og ilt?
Næste artikelHvad gør ammoniak i Hill Reaction Lab?
 Varme artikler
Varme artikler
-
 Økolim kan erstatte skadelige klæbemidler i træbyggeriKredit:Aalto Universitet Forskere ved Aalto Universitetet har udviklet en biobaseret klæbemiddel, der kan erstatte formaldehydholdige klæbemidler i træbyggeri. Det vigtigste råmateriale i den nye l
Økolim kan erstatte skadelige klæbemidler i træbyggeriKredit:Aalto Universitet Forskere ved Aalto Universitetet har udviklet en biobaseret klæbemiddel, der kan erstatte formaldehydholdige klæbemidler i træbyggeri. Det vigtigste råmateriale i den nye l -
 Forudsigelse af sekvens fra strukturBindingsgrænsefladen mellem et peptid og dets Bcl-2-proteinmål er sammensat af almindelige strukturelle motiver kendt som TERMer. Kredit:Sebastian Swanson og Avi Singer En måde at undersøge indvik
Forudsigelse af sekvens fra strukturBindingsgrænsefladen mellem et peptid og dets Bcl-2-proteinmål er sammensat af almindelige strukturelle motiver kendt som TERMer. Kredit:Sebastian Swanson og Avi Singer En måde at undersøge indvik -
 Ny undersøgelse af biofilm kan føre til en mere bæredygtig vandindustriKredit:Pixabay/CC0 Public Domain En lille reduktion af mængden af rester af desinfektionsmiddel, vi bruger til at vedligeholde rent drikkevand, kan give betydelige forbedringer af vandkvaliteten
Ny undersøgelse af biofilm kan føre til en mere bæredygtig vandindustriKredit:Pixabay/CC0 Public Domain En lille reduktion af mængden af rester af desinfektionsmiddel, vi bruger til at vedligeholde rent drikkevand, kan give betydelige forbedringer af vandkvaliteten -
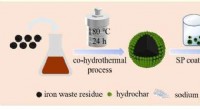 Forskere bruger tobaksaffaldsvæske og jernrester til fjernelse af Cd(II)Skematisk diagram af fremstillingsprocessen og adsorptionsmekanismerne for OWIR@TWL@SP. Kredit:WU Qingchuan Ifølge en ny undersøgelse offentliggjort i Langmuir , blev en slags jernbaseret kulstofmi
Forskere bruger tobaksaffaldsvæske og jernrester til fjernelse af Cd(II)Skematisk diagram af fremstillingsprocessen og adsorptionsmekanismerne for OWIR@TWL@SP. Kredit:WU Qingchuan Ifølge en ny undersøgelse offentliggjort i Langmuir , blev en slags jernbaseret kulstofmi
- Det biologisk nedbrydelige batteri, der er 3D-printet, engangs og lavet af papir
- Hvordan glat vand og sort skifer i fracking kombineres for at producere radioaktivt affald
- Forskere søger at aflede asteroider, forhindrer deres kollision med Jorden
- At overleve en zombieapokalypse ved hjælp af matematik
- Livet på Jorden er vant til tyngdekraften - så hvad sker der med vores celler og væv i rummet?
- De otte mest rigelige elementer i jordskorpen


