Hvad er oxidationstilstanden for svovl?
* mest almindelige oxidation siger:
* -2: Fundet i mange sulfider som H₂s, Na₂s og FES.
* +4: Fundet i forbindelser som SO₂ (svovldioxid) og H₂so₃ (svovlsyre).
* +6: Fundet i forbindelser som SO₃ (svovltrioxid) og H₂so₄ (svovlsyre).
* Andre oxidationstilstande: Svovl kan også have oxidationstilstande på +1, +2 og +3, men disse er mindre almindelige.
hvordan man bestemmer oxidationstilstanden for svovl:
1. Husk reglerne: Oxygen har normalt en oxidationstilstand på -2, brint er +1 (undtagen i metalhydrider), og summen af alle oxidationstilstande i en forbindelse skal svare til nul.
2. Anvend reglerne: For eksempel er ilt -2 i So₂ -2, så to iltatomer har en samlet ladning på -4. For at afbalancere dette skal svovl have en +4 oxidationstilstand.
Fortæl mig, hvis du vil udforske specifikke eksempler!
Sidste artikelHvad er formlen for molekylær forbindelsesfosfor pentachlorid?
Næste artikelOpløses svovlpulver i vand?
 Varme artikler
Varme artikler
-
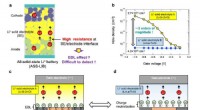 Ny måde at undersøge den elektriske dobbeltlagseffekt på(a) Diagram over et hel-solid-state Li-ion batteri, der lider af høj grænseflademodstand, formodes at skyldes EDL-effekten. (b) Diamantbaserede felteffekttransistorer (FETer) lader os modulere huldens
Ny måde at undersøge den elektriske dobbeltlagseffekt på(a) Diagram over et hel-solid-state Li-ion batteri, der lider af høj grænseflademodstand, formodes at skyldes EDL-effekten. (b) Diamantbaserede felteffekttransistorer (FETer) lader os modulere huldens -
 Molekylelag hjælper med kemoselektiv hydrogenering på faste palladiumkatalysatorerKredit:Wiley Kemiske reaktioner går ikke altid efter planen. Uønskede biprodukter fører til ekstra omkostninger og ressourcespild. Selektive katalysatorer kan hjælpe, men kemikere skal afprøve sto
Molekylelag hjælper med kemoselektiv hydrogenering på faste palladiumkatalysatorerKredit:Wiley Kemiske reaktioner går ikke altid efter planen. Uønskede biprodukter fører til ekstra omkostninger og ressourcespild. Selektive katalysatorer kan hjælpe, men kemikere skal afprøve sto -
 Enzym kan få en nøglerolle i lægemiddeldesign til brystkræft og hjernesygdomKredit:Københavns Universitet I de seneste år, forskere har fokuseret på enzymet TLK2, mistænkes for at spille en hovedrolle i flere sygdomme. En ny undersøgelse foretaget på Københavns Universite
Enzym kan få en nøglerolle i lægemiddeldesign til brystkræft og hjernesygdomKredit:Københavns Universitet I de seneste år, forskere har fokuseret på enzymet TLK2, mistænkes for at spille en hovedrolle i flere sygdomme. En ny undersøgelse foretaget på Københavns Universite -
 Hvordan interstitiel bestilling påvirker højstyrkestålKredit:CC0 Public Domain Materialers ydeevne er stærkt påvirket af deres legeringselementer:Tilføjelse af elementer ud over legeringens grundlæggende sammensætning kan i høj grad påvirke egenskabe
Hvordan interstitiel bestilling påvirker højstyrkestålKredit:CC0 Public Domain Materialers ydeevne er stærkt påvirket af deres legeringselementer:Tilføjelse af elementer ud over legeringens grundlæggende sammensætning kan i høj grad påvirke egenskabe
- Hvad er hver halvdel af Jorden opdelt enten nord- og syd- eller østvest?
- Hvilken type bevægelse ville producere positiv acceleration i et objekt?
- Byplanlægning lider under vækstsmerter af Australiens befolkningsboom
- Er sved en isolator af elektricitet?
- Computere hjælper med at opdage nye, billigt materiale til at lave LED'er med høj farvekvalitet
- Hvordan man hæver medicinsk grad lege


