Er benzen reaktiv med brom i mørke?
Her er hvorfor:
* benzens stabilitet: Benzen er en aromatisk forbindelse med en meget stabil struktur på grund af dens delokaliserede elektroner. Denne stabilitet gør det relativt ureaktivt.
* Bromes elektrofile karakter: Brom er en elektrofil, hvilket betyder, at den søger elektroner.
* behovet for en katalysator: Reaktionen af benzen med brom kræver en katalysator, typisk en Lewis -syre som jern (III) bromid (februar). Denne katalysator hjælper med at generere en mere reaktiv elektrofil (bromoniumion), der kan angribe den elektronrige benzenring.
I mangel af en katalysator og lys forekommer reaktionen mellem benzen og brom ikke.
Men hvis den udsættes for lys, Reaktionen kan fortsætte via en fri radikal mekanisme , men denne reaktion er meget langsommere end den katalyserede reaktion og producerer en blanding af produkter, herunder bromobenzen og polybromerede benzener.
 Varme artikler
Varme artikler
-
 Find de faktorer, der påvirker stålkorrosionen mest i armeret beton mestMercedes Sánchez, undersøgelse af undersøgelsen. Kredit:Universidad de Córdoba Siden de egyptiske pyramider og det romerske Colosseum blev bygget, menneskeheden har ledt efter en overkommelig pris
Find de faktorer, der påvirker stålkorrosionen mest i armeret beton mestMercedes Sánchez, undersøgelse af undersøgelsen. Kredit:Universidad de Córdoba Siden de egyptiske pyramider og det romerske Colosseum blev bygget, menneskeheden har ledt efter en overkommelig pris -
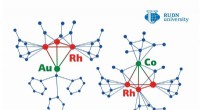 Kemikere foreslår en metode til fremstilling af metalbaserede katalysatorer med uovertruffen effekt…Kredit:RUDN Universitet Et team af kemikere fra RUDN University og Nesmeyanov Institute of Organoelement Compounds (INEOS) syntetiserede to heterometalliske klynger med næsten 100 % effektivitet.
Kemikere foreslår en metode til fremstilling af metalbaserede katalysatorer med uovertruffen effekt…Kredit:RUDN Universitet Et team af kemikere fra RUDN University og Nesmeyanov Institute of Organoelement Compounds (INEOS) syntetiserede to heterometalliske klynger med næsten 100 % effektivitet. -
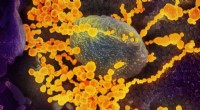 Forskere viser, at selvsteriliserende polymerer virker mod SARS-CoV-2Dette scanningselektronmikroskopbillede viser SARS-CoV-2 (runde guldobjekter), der dukker op fra overfladen af celler dyrket i laboratoriet. Kredit:NIAID-RML Forskere fra North Carolina State Un
Forskere viser, at selvsteriliserende polymerer virker mod SARS-CoV-2Dette scanningselektronmikroskopbillede viser SARS-CoV-2 (runde guldobjekter), der dukker op fra overfladen af celler dyrket i laboratoriet. Kredit:NIAID-RML Forskere fra North Carolina State Un -
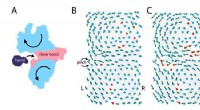 Sådan kodes en funktionel molekylær maskineFigur 1:Elastisk model af et protein, der binder til en ligand. (A) Når et protein binder til en ligand, det gennemgår store bevægelser (pile), som er signaturerne for bøjede funktionelle proteiner. D
Sådan kodes en funktionel molekylær maskineFigur 1:Elastisk model af et protein, der binder til en ligand. (A) Når et protein binder til en ligand, det gennemgår store bevægelser (pile), som er signaturerne for bøjede funktionelle proteiner. D
- Ved nærmere eftertanke, Månens vand kan være udbredt og ubevægeligt
- Hvilken størrelse solpanel vil forsyne 1000 watt i 24 timer?
- Forskere viser, at oliepalmeplantager rydder kulstofrige tropiske skove på Borneo
- Hvor er de ædle gasser på periodisk talde?
- Hvilket fly har ingen måner?
- Hvordan ændres partiklernes opførsel, når energi tilføjes?


