Hvorfor ville det være usandsynligt, at et fast materiale er lavet af rene carbonationer?
* Gebyr ubalance: Carbonationer har en -2 -ladning. For at danne en neutral forbindelse skal de være afbalanceret med positive ladninger. Et solidt materiale, der udelukkende er fremstillet af carbonationer, ville have en massiv samlet negativ ladning, hvilket er energisk ugunstigt.
* ustabilitet: Carbonationer er i sagens natur ustabile på egen hånd. De har en tendens til at reagere med andre ioner eller molekyler for at opnå en mere stabil tilstand.
* ionisk binding: Carbonationer er typisk involveret i ionisk binding, hvor de interagerer med positivt ladede ioner (kationer) for at danne salte. Disse salte er stabile på grund af den elektrostatiske tiltrækning mellem de modsatte ladninger.
Eksempler:
* calciumcarbonat (caco₃): Et almindeligt eksempel på en carbonatforbindelse, hvor +2 ladning af calciumioner afbalancerer -2 -ladningen for carbonationer.
* natriumcarbonat (Na₂co₃): Et andet eksempel, hvor to +1 natriumioner afbalancerer -2 -ladningen af carbonationen.
Afslutningsvis, mens carbonationer er en vigtig del af mange forbindelser, er det meget usandsynligt, at de eksisterer uafhængigt i en fast tilstand på grund af ladning af ubalance og iboende ustabilitet.
Sidste artikelKuldioxid reagerer med vand at dannes?
Næste artikelHvad var de første fire elementer, der blev brugt i kemi?
 Varme artikler
Varme artikler
-
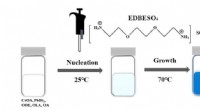 En ny strategi til at skabe blåt lys fra et lovende materialeSkemaet for syntesen af EDBESO4 behandlet CsPbBr3 NPLer. Kredit:Avancerede energimaterialer DOI:10.1002/aenm.202201605 Et forskningshold fra Florida State University har udviklet en ny måde at sk
En ny strategi til at skabe blåt lys fra et lovende materialeSkemaet for syntesen af EDBESO4 behandlet CsPbBr3 NPLer. Kredit:Avancerede energimaterialer DOI:10.1002/aenm.202201605 Et forskningshold fra Florida State University har udviklet en ny måde at sk -
 Nyudviklede udviklede enzymer producerer vedvarende isobutenKredit:University of Manchester Ny forskning offentliggjort i dag beskriver et gennembrud i skabelsen af udviklede enzymer til at understøtte en vedvarende proces til at lave en af de vigtigst
Nyudviklede udviklede enzymer producerer vedvarende isobutenKredit:University of Manchester Ny forskning offentliggjort i dag beskriver et gennembrud i skabelsen af udviklede enzymer til at understøtte en vedvarende proces til at lave en af de vigtigst -
 En sorteringsteknologi, der isolerer celler med høj renhed og levedygtighedEt kappeløst akustisk fluorescensaktiveret cellesorteringssystem (aFACS) til isolering af skrøbelige biologiske celler med høj cellerenhed og levedygtighed. Kredit:SUTD Fluorescensaktiveret celles
En sorteringsteknologi, der isolerer celler med høj renhed og levedygtighedEt kappeløst akustisk fluorescensaktiveret cellesorteringssystem (aFACS) til isolering af skrøbelige biologiske celler med høj cellerenhed og levedygtighed. Kredit:SUTD Fluorescensaktiveret celles -
 Ultrahurtige lasere sonderer undvigende kemi ved væske-væske-grænsefladenForskere ved Oak Ridge National Laboratory kaster nyt lys over undvigende kemiske processer ved væske-væske grænsefladen under opløsningsmiddelekstraktion af kobolt, vist i mørkeblå. Kredit:Michelle L
Ultrahurtige lasere sonderer undvigende kemi ved væske-væske-grænsefladenForskere ved Oak Ridge National Laboratory kaster nyt lys over undvigende kemiske processer ved væske-væske grænsefladen under opløsningsmiddelekstraktion af kobolt, vist i mørkeblå. Kredit:Michelle L


