Hvordan blev stigende temperatur på opløsningsmiddelforandringshastighed, hvormed kobbersulfat opløstes i vand?
* Øget kinetisk energi: Højere temperaturer betyder, at vandmolekyler har mere kinetisk energi og bevæger sig hurtigere. Denne øgede bevægelse fører til:
* hyppigere kollisioner: Vandmolekyler kolliderer oftere med kobbersulfatkrystaller.
* flere energiske kollisioner: Kollisionerne er mere kraftfulde og bryder bindingerne fra hinanden, der holder kobbersulfatkrystaller sammen.
* svækkede intermolekylære kræfter: Varme svækker de intermolekylære kræfter (brintbindinger) mellem vandmolekyler. Dette gør det muligt for vandmolekyler lettere at omringe og interagere med kobbersulfationer og bryde dem væk fra krystalgitteret.
i enklere termer: Forestil dig kobbersulfatkrystaller som en gruppe mennesker, der holder hænderne tæt. Vandmolekylerne er som dansere, der prøver at trække dem fra hinanden. Varmere vand betyder, at danserne er mere energiske og vedvarende, hvilket gør det meget lettere at bryde gruppen fra hinanden.
Yderligere faktorer:
* opløselighed: Mens højere temperaturer øger opløsningens * hastighed *, øger de også generelt * opløselighed * af kobbersulfat. Dette betyder, at mere kobbersulfat kan opløses i en given mængde vand ved højere temperaturer.
Vigtig note: Opløseligheden af kobbersulfat er begrænset. Selv med høje temperaturer er der et maksimalt beløb, der opløses i et givet volumen vand.
Sidste artikelHvorfor er en nitration stærkere base end sulfidion?
Næste artikelHvad er formålet med svovl i brændstof?
 Varme artikler
Varme artikler
-
 Forskere præsenterer en ny tilgang til overvågning af ferskvands sundhedMinION er en bærbar enhed, der kan sekvensere genetisk materiale, der er taget fra miljøet - her, fra River Cam i Cambridge, Storbritannien. Kredit:Team PuntSeq (CC BY 4.0) Forskere har brugt verd
Forskere præsenterer en ny tilgang til overvågning af ferskvands sundhedMinION er en bærbar enhed, der kan sekvensere genetisk materiale, der er taget fra miljøet - her, fra River Cam i Cambridge, Storbritannien. Kredit:Team PuntSeq (CC BY 4.0) Forskere har brugt verd -
 Egenskaber af katalysatorer studeret med gammastråleresonansKredit:Kazan Federal University Dampstøttede olieudvindingsmetoder til tunge aflejringer har længe været i fokus på Kazan Federal University. I særdeleshed, Der lægges stor vægt på in-situ forbræn
Egenskaber af katalysatorer studeret med gammastråleresonansKredit:Kazan Federal University Dampstøttede olieudvindingsmetoder til tunge aflejringer har længe været i fokus på Kazan Federal University. I særdeleshed, Der lægges stor vægt på in-situ forbræn -
 Kæmpe ladningsomvendelse observeret for første gangSnapshots til distribution af ioner nær en negativt ladet plan overflade ved forskellige dielektriske kontraster. Kredit:Jianzhong Wu, University of California, Riverside Ladede overflader nedsænk
Kæmpe ladningsomvendelse observeret for første gangSnapshots til distribution af ioner nær en negativt ladet plan overflade ved forskellige dielektriske kontraster. Kredit:Jianzhong Wu, University of California, Riverside Ladede overflader nedsænk -
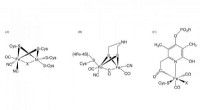 CO-biosyntese påkrævet til samling af det aktive sted i NiFe-hydrogenaseFigur 1. Struktur af de aktive steder i [NiFe] -hydrogenase, [FeFe] -hydrogenase, og [Fe] -hydrogenase Kredit:NINS/IMS En forskergruppe, der omfatter forskere fra Exploratory Research Center on Li
CO-biosyntese påkrævet til samling af det aktive sted i NiFe-hydrogenaseFigur 1. Struktur af de aktive steder i [NiFe] -hydrogenase, [FeFe] -hydrogenase, og [Fe] -hydrogenase Kredit:NINS/IMS En forskergruppe, der omfatter forskere fra Exploratory Research Center on Li
- Den oprindelige befolkning på det gamle Sicilien var aktive handlende
- Forskere bruger en virus til at fremskynde moderne computere
- Hvordan kan du fysisk adskille en blanding af jernfyldningstabel salt og hvidt sand?
- Nye selvdrevne nanopartikler udviklet til at levere helbredende lægemidler direkte til knoglespræk…
- Er svovlmagnetisk eller ikke magnetisk?
- Hvad er genetisk videnskab?


