Overskydende iltgas blandes med ammoniak i nærvær af platin?
Her er den afbalancerede kemiske ligning:
4 NH₃ (G) + 5 O₂ (G) → 4 Nej (G) + 6 H₂O (G)
Forklaring:
* platin fungerer som en katalysator: Det fremskynder reaktionen uden at blive fortæret selv. Platin tilvejebringer en overflade til ammoniak- og iltmolekyler til adsorber og reagerer mere effektivt.
* overskydende ilt: Tilstedeværelsen af overskydende ilt sikrer, at al ammoniak oxideres.
* eksotermisk reaktion: Reaktionen frigiver en betydelig mængde varme, hvorfor den undertiden bruges i industrielle processer.
Vigtig note:
Denne reaktion er et afgørende trin i ostwald -processen , en vigtig industriel proces til produktion af salpetersyre. Salpetersyre er et vigtigt kemikalie, der bruges til produktion af gødning, sprængstoffer og andre kemikalier.
bivirkninger:
Det er værd at bemærke, at der under forskellige forhold eller med forskellige katalysatorer kan forekomme andre reaktioner. For eksempel kan nitrogenoxider (NOX) dannes, som er forurenende stoffer. Under de betingelser, der er beskrevet i prompten, er den primære reaktion imidlertid dannelsen af nitrogengas og vand.
Sidste artikelHvor kommer protonsneutroner og elektroner fra?
Næste artikelHvad sker der, når brint reagerer med kobberoxid?
 Varme artikler
Varme artikler
-
 De vigtigste materialer og enheder til iboende fleksible skærmeTeknisk set er der forskellige veje til realisering af fleksibilitet. 1) Fysisk fleksibilitet:ethvert stift materiale, der er ekstremt tyndt eller har en meget lille diameter, kan være fleksibelt. 2)
De vigtigste materialer og enheder til iboende fleksible skærmeTeknisk set er der forskellige veje til realisering af fleksibilitet. 1) Fysisk fleksibilitet:ethvert stift materiale, der er ekstremt tyndt eller har en meget lille diameter, kan være fleksibelt. 2) -
 Afdækning af hemmelighederne bag materialenedbrydning i et lithium-ion-batteriSkematisk diagram af KIST batterianalyseplatform. Kredit:Korea Institute of Science and Technology (KIST) Midt i den globale indsats for CO2-neutralitet er bilproducenter over hele verden aktivt en
Afdækning af hemmelighederne bag materialenedbrydning i et lithium-ion-batteriSkematisk diagram af KIST batterianalyseplatform. Kredit:Korea Institute of Science and Technology (KIST) Midt i den globale indsats for CO2-neutralitet er bilproducenter over hele verden aktivt en -
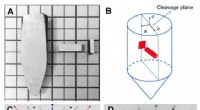 Høj termoelektrisk ydeevne i billige SnS0.91Se0.09-krystaller(A) En typisk krystal spaltet langs (100) planet, og prøve skåret langs b-aksen. (B) Et diagram viser, hvordan prøver skærer langs b-aksen til målinger. (C) Standard Laue diffraktionsbillede af SnS kr
Høj termoelektrisk ydeevne i billige SnS0.91Se0.09-krystaller(A) En typisk krystal spaltet langs (100) planet, og prøve skåret langs b-aksen. (B) Et diagram viser, hvordan prøver skærer langs b-aksen til målinger. (C) Standard Laue diffraktionsbillede af SnS kr -
 Slip sukkeret! En værdifuld byggesten til fremstilling af produkter af madaffaldKredit:CENER Næsten halvdelen af det, vi smider, er organisk affald - bananskind, et par rester ... De fleste byer indsamler denne type affald adskilt fra husholdninger. Men meget få byer gør go
Slip sukkeret! En værdifuld byggesten til fremstilling af produkter af madaffaldKredit:CENER Næsten halvdelen af det, vi smider, er organisk affald - bananskind, et par rester ... De fleste byer indsamler denne type affald adskilt fra husholdninger. Men meget få byer gør go
- Hvilken termodynamisk proces giver maksimalt arbejde?
- Hvordan ser en fossil ud?
- Krig mod plastik får producenterne til at gribe om sugerør
- Ideer til videnskabsretlige projekter på Fish
- Mekanisme bag XFEL-induceret smeltning af diamant afsløret
- Hvad kan du konkludere, hvis der placeres Nordpolen i en stangmagnet nær en umærket, og de afviser…


