Hvilken lov beskriver forholdet mellem volumen og temperatur på en gas, når trykket er konstant?
Charles 'lov siger, at mængden af en fast gasmasse er direkte proportional med dens absolutte temperatur, når trykket holdes konstant.
Matematisk kan det udtrykkes som:
v₁/t₁ =v₂/t₂
Hvor:
* V₁ er det oprindelige bind
* T₁ er den oprindelige absolutte temperatur (i Kelvin)
* V₂ er det endelige bind
* T₂ er den endelige absolutte temperatur (i Kelvin)
Dette betyder, at hvis du øger temperaturen på en gas, vil dens volumen stige proportionalt, så længe trykket forbliver konstant. Omvendt, hvis du reducerer temperaturen, vil volumenet falde proportionalt.
 Varme artikler
Varme artikler
-
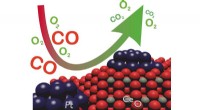 Dynamiske katalysatorer til ren luft i byenEn bils katalysator omdanner giftigt kulilte (CO) til giftfri kuldioxid (CO2) og består af cerium (Ce), ilt (O), og platin (Pt). Kredit:Gänzler/KIT Reduktion af forurenende emissioner af køretøjer
Dynamiske katalysatorer til ren luft i byenEn bils katalysator omdanner giftigt kulilte (CO) til giftfri kuldioxid (CO2) og består af cerium (Ce), ilt (O), og platin (Pt). Kredit:Gänzler/KIT Reduktion af forurenende emissioner af køretøjer -
 Gør havvand drikkeligt på få minutterSkematisk oversigt over koaksial elektrospinning. Kredit:Elsevier Ifølge Verdenssundhedsorganisationen omkring 785 millioner mennesker rundt om i verden mangler en ren drikkevandskilde. På trods a
Gør havvand drikkeligt på få minutterSkematisk oversigt over koaksial elektrospinning. Kredit:Elsevier Ifølge Verdenssundhedsorganisationen omkring 785 millioner mennesker rundt om i verden mangler en ren drikkevandskilde. På trods a -
 Hvordan en svamp kan ødelægge immunsystemetSvampen Aspergillus fumigatus er overalt, og er ekstremt farlig for mennesker med svækket immunsystem. Det forekommer stort set overalt på Jorden, som en mørkegrå plet på fugtige vægge eller i mikrosk
Hvordan en svamp kan ødelægge immunsystemetSvampen Aspergillus fumigatus er overalt, og er ekstremt farlig for mennesker med svækket immunsystem. Det forekommer stort set overalt på Jorden, som en mørkegrå plet på fugtige vægge eller i mikrosk -
 Ny forskning har til formål at afdække smertestillende hemmeligheder bag dødelig sneglegiftKeglesnegl (Conasprella jaspidea pealii) spiser en ildorm. Kredit:Rickard Zerpe/Wikimedia Commons, CC BY-SA 2.0 Den dødelige gift fra en giftig havsnegl kan være nøglen til at udvikle ny medicin, h
Ny forskning har til formål at afdække smertestillende hemmeligheder bag dødelig sneglegiftKeglesnegl (Conasprella jaspidea pealii) spiser en ildorm. Kredit:Rickard Zerpe/Wikimedia Commons, CC BY-SA 2.0 Den dødelige gift fra en giftig havsnegl kan være nøglen til at udvikle ny medicin, h
- Hvordan kan et atom blive elektrisk ladet?
- Rockefeller Collection solgte for rekordstore 832 millioner dollars
- Hvad er den første fase af cellulær respiration og ældste med hensyn til evolution?
- Hvad er det beløb, hvormed hastighed stiger på et sekund, der kaldes?
- Hvorfor er der næsten ingen ekstruderende ultra-basiske klipper i jordskorpe?
- Hvordan LinkedIns søgemaskine kan afspejle en kønsbias


