Forholdet mellem tryk og volumen af en gas ved konstant temperatur gives af?
Boyle's Law siger, at produktet af tryk og volumen af en gas er konstant ved en konstant temperatur .
Matematisk kan dette udtrykkes som:
p₁v₁ =p₂v₂
hvor:
* P₁ er det oprindelige pres
* V₁ er det oprindelige bind
* P₂ er det endelige pres
* V₂ er det endelige bind
Forklaring:
Denne lov indebærer, at hvis trykket fra en gas øges, falder dens volumen forholdsmæssigt, og vice versa, mens temperaturen forbliver konstant. Dette skyldes, at gasmolekylerne har en konstant kinetisk energi ved konstant temperatur. Efterhånden som trykket øges, kolliderer molekylerne med containervæggene hyppigere, hvilket resulterer i et fald i volumen for at opretholde den samme kinetiske energi.
 Varme artikler
Varme artikler
-
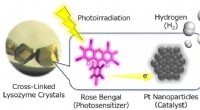 Forskere bruger æggehvider til ren energiproduktionHydrogen (H2) udviklingssystemer konstrueret i tværbundne porøse lysozymkrystaller ved at immobilisere Pt-nanopartikler som H2-evolutionskatalysatorer i umiddelbar nærhed af en organisk fotosensibilis
Forskere bruger æggehvider til ren energiproduktionHydrogen (H2) udviklingssystemer konstrueret i tværbundne porøse lysozymkrystaller ved at immobilisere Pt-nanopartikler som H2-evolutionskatalysatorer i umiddelbar nærhed af en organisk fotosensibilis -
 Ny bærerdoping i p-type halvledere forbedrer fotovoltaisk enheds ydeevne ved at øge hulkoncentrati…Grafisk abstrakt. Kredit:Tokyo Tech Perovskite-solceller har været genstand for megen forskning som den næste generation af solceller. Der er dog stadig mange udfordringer, der skal overvindes for
Ny bærerdoping i p-type halvledere forbedrer fotovoltaisk enheds ydeevne ved at øge hulkoncentrati…Grafisk abstrakt. Kredit:Tokyo Tech Perovskite-solceller har været genstand for megen forskning som den næste generation af solceller. Der er dog stadig mange udfordringer, der skal overvindes for -
 Praktisk antioxidantkapacitetsmåling af madNormalt, en prøve opløses i en elektrolytopløsning og tre elektroder (virkende, reference, tæller) indsættes i opløsningen for at udføre elektrokemiske målinger. I dette system, imidlertid, der er ing
Praktisk antioxidantkapacitetsmåling af madNormalt, en prøve opløses i en elektrolytopløsning og tre elektroder (virkende, reference, tæller) indsættes i opløsningen for at udføre elektrokemiske målinger. I dette system, imidlertid, der er ing -
 Neutronundersøgelse af glaukomlægemidler giver fingerpeg om enzymmål for aggressive kræftformerDet aktive sted for hCA II. Det aktive sted er flankeret af hydrofile (violette) og hydrofobe (grønne) bindingslommer, der kan bruges til at designe specifikke lægemidler rettet mod cancer-associerede
Neutronundersøgelse af glaukomlægemidler giver fingerpeg om enzymmål for aggressive kræftformerDet aktive sted for hCA II. Det aktive sted er flankeret af hydrofile (violette) og hydrofobe (grønne) bindingslommer, der kan bruges til at designe specifikke lægemidler rettet mod cancer-associerede
- Ny teknologi øger dramatisk genindvindingsgraden af ædle metaller fra affald
- Betyr et større mAh-nummer på dit mobiltelefon batteri et bedre batteri?
- Økologer foreslår, at det er tid til at gentænke den moderne græsplæne
- Fra mælkeprotein, et plastikskum, der bliver bedre i et hårdt miljø
- Hvad er en sol i skabelsen kaldet?
- Kan en første kvartal ocour under Toltal Solar Eclipse?


