Hvorfor udvides stoffer, når temperaturen øges?
* kinetisk energi og molekylær bevægelse: Molekyler i et stof er konstant i bevægelse. Denne bevægelse kaldes kinetisk energi.
* Temperatur og kinetisk energi: Temperaturen er et mål for den gennemsnitlige kinetiske energi af molekylerne i et stof. Højere temperatur betyder, at molekylerne bevæger sig hurtigere.
* Øget afstand: Når molekylerne bevæger sig hurtigere, kolliderer de med hinanden hyppigere og med større kraft. Denne øgede kollisionskraft skubber molekylerne længere fra hinanden, hvilket fører til en ekspansion i stoffet.
Tænk på det sådan: Forestil dig en gruppe mennesker i et overfyldt rum. Hvis alle står stille, kan de passe ind i et mindre rum. Men hvis alle begynder at bevæge sig hurtigt, har de brug for mere plads for at undgå at støde på hinanden. Det samme princip gælder for molekyler i et stof.
Typer af ekspansion:
* lineær ekspansion: Dette henviser til udvidelsen af et stof i en dimension, som længden af en metalstang.
* Områdeudvidelse: Dette henviser til udvidelsen af et stof i to dimensioner, som overfladearealet i et metalplade.
* Volumenudvidelse: Dette henviser til udvidelsen af et stof i tre dimensioner, som mængden af en beholder med vand.
Undtagelser:
Mens de fleste stoffer ekspanderer, når de opvarmes, er der nogle undtagelser, som vand mellem 0 ° C og 4 ° C. I dette temperaturområde sammentrækker vand faktisk lidt efter opvarmning. Denne usædvanlige opførsel skyldes de unikke egenskaber ved vandmolekyler og deres hydrogenbinding.
Fortæl mig, hvis du gerne vil have flere detaljer om nogen af disse aspekter!
Sidste artikelHvad er de vigtigste måde, molekyler bevæger sig på?
Næste artikelHvad kaldes væske, når et solidt?
 Varme artikler
Varme artikler
-
 Elektronisk entropi forbedrer vandspaltningKredit:George Hodan/public domain Forskere har længe vidst, at cerium er det bedste element at bruge, når man spalter vand til brint og ilt - en nøgleteknik til at skabe brintgas til brændstof. Me
Elektronisk entropi forbedrer vandspaltningKredit:George Hodan/public domain Forskere har længe vidst, at cerium er det bedste element at bruge, når man spalter vand til brint og ilt - en nøgleteknik til at skabe brintgas til brændstof. Me -
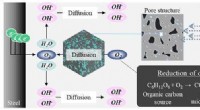 Korrosionsbestandighed af stålstænger i beton, når de blandes med aerobe mikroorganismerEt skematisk billede af indtrængen af ilt i porestrukturen og reduktion af opløst ilt af aerobe mikroorganismer i poreopløsning. Kredit:Ehime University Opløst oxygen i poreopløsning er ofte en
Korrosionsbestandighed af stålstænger i beton, når de blandes med aerobe mikroorganismerEt skematisk billede af indtrængen af ilt i porestrukturen og reduktion af opløst ilt af aerobe mikroorganismer i poreopløsning. Kredit:Ehime University Opløst oxygen i poreopløsning er ofte en -
 Eksperimentelle fysikere studerer stål om bord på ISSPeter Pichler (tv) med arbejdsgruppeleder Gernot Pottlacher (th.). Fra stålstangen i deres hænder, de skar de små bolde, som nu bliver undersøgt på ISS. Kredit:Baustädter - TU Graz I mange år, Ins
Eksperimentelle fysikere studerer stål om bord på ISSPeter Pichler (tv) med arbejdsgruppeleder Gernot Pottlacher (th.). Fra stålstangen i deres hænder, de skar de små bolde, som nu bliver undersøgt på ISS. Kredit:Baustädter - TU Graz I mange år, Ins -
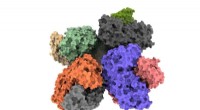 Ny indsigt i fermenteringsenzymer vil sænke den kemiske industris CO2-fodaftrykForskere fra University of Tsukuba har opnået indsigt på atomniveau i strukturen af phosphoketolase-enzymet, hvilket vil hjælpe forskere med at optimere dette enzym til kemisk råstofsyntese. Kredit:
Ny indsigt i fermenteringsenzymer vil sænke den kemiske industris CO2-fodaftrykForskere fra University of Tsukuba har opnået indsigt på atomniveau i strukturen af phosphoketolase-enzymet, hvilket vil hjælpe forskere med at optimere dette enzym til kemisk råstofsyntese. Kredit:
- Hvad er forholdet mellem DNA RNA og proteinsyntese?
- Hvordan kan mineralsammensætning påvirke farven på en stødende klippe?
- Forskere får et hidtil uset syn på bestrålet atombrændstof
- Små fiskeri tilbyder strategier for modstandsdygtighed over for klimaændringer
- Beskyttelse af oprindelige kulturer er afgørende for at redde verdens biodiversitet
- Hvad er et andet ord for raffineret?


