Hvad sker der med tætheden af en afkølet væske?
* termisk ekspansion: Væsker, som de fleste stoffer, udvides, når de opvarmes og sammentrækkes, når de afkøles. Dette skyldes, at molekylerne bevæger sig hurtigere og optager mere plads ved højere temperaturer.
* densitet: Densitet defineres som masse pr. Enhedsvolumen. Når en væske afkøles, falder dens volumen (kontrakter), mens dens masse forbliver den samme. Da den samme mængde masse nu optager et mindre volumen, øges densiteten.
Undtagelser:
Der er nogle få undtagelser fra denne regel, hovedsageligt relateret til vand:
* Vands anomal opførsel: Vand er usædvanligt, fordi dens densitet når et maksimum ved 4 ° C (39,2 ° F). Når vandet afkøles yderligere, falder dens densitet lidt. Dette skyldes dannelsen af brintbindinger, der får vandmolekylerne til at arrangere sig i en mindre kompakt struktur. Dette er grunden til, at is flyder på vandet!
Kortfattet:
For de fleste væsker fører afkøling til en stigning i densitet. Imidlertid udviser vand en unik opførsel, hvor dens densitet toppe ved 4 ° C, hvilket gør det tættere end is.
Sidste artikelVil materialerne, der flyder på vandet, også olie?
Næste artikelNår vand afkøles, hvad sker der med densiteten?
 Varme artikler
Varme artikler
-
 Højteknologisk materiale i en saltskorpeDr. Jesus Gonzalez-Julian (til højre) og Apurv Dash (til venstre). Kredit:Forschungszentrum Jülich / Regine Panknin MAX faser betragtes som lovende materialer for fremtiden, for eksempel, i magten
Højteknologisk materiale i en saltskorpeDr. Jesus Gonzalez-Julian (til højre) og Apurv Dash (til venstre). Kredit:Forschungszentrum Jülich / Regine Panknin MAX faser betragtes som lovende materialer for fremtiden, for eksempel, i magten -
 Forskere optrævler flere mysterier af metallisk brintMetallisk brint er et af de sjældneste materialer på jorden, men det udgør mere end 80 procent af planeter som Jupiter. Forskere ved University of Rochesters Laboratory for Laser Energetics skabte met
Forskere optrævler flere mysterier af metallisk brintMetallisk brint er et af de sjældneste materialer på jorden, men det udgør mere end 80 procent af planeter som Jupiter. Forskere ved University of Rochesters Laboratory for Laser Energetics skabte met -
 Gør havvand drikkeligt på få minutterSkematisk oversigt over koaksial elektrospinning. Kredit:Elsevier Ifølge Verdenssundhedsorganisationen omkring 785 millioner mennesker rundt om i verden mangler en ren drikkevandskilde. På trods a
Gør havvand drikkeligt på få minutterSkematisk oversigt over koaksial elektrospinning. Kredit:Elsevier Ifølge Verdenssundhedsorganisationen omkring 785 millioner mennesker rundt om i verden mangler en ren drikkevandskilde. På trods a -
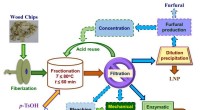 Delignificering af træprøver ved hjælp af p-toluensulfonsyre som en genanvendelig hydrotropSkematisk flowdiagram viser træfraktionering ved hjælp af p-TsOH til produktion af fibre, lignocellulosiske nanomaterialer, sukker, og LNPer. Processer med stiplede linjer blev ikke udført i denne und
Delignificering af træprøver ved hjælp af p-toluensulfonsyre som en genanvendelig hydrotropSkematisk flowdiagram viser træfraktionering ved hjælp af p-TsOH til produktion af fibre, lignocellulosiske nanomaterialer, sukker, og LNPer. Processer med stiplede linjer blev ikke udført i denne und
- Hvordan påvirker kinetisk energi diffusionshastighed?
- Hvordan FN's nye åbne videnskabsramme kunne fremskynde opdagelsestempoet
- Tyve års planetarisk forsvar
- Hvorfor er klippen fra Mid Atlantic Ridge yngre end fundet på kantkontinenter?
- Hvad er udånding og indånding?
- Er kogning af mælk et eksempel eksotermisk proces?


