Når gas i en beholder udvides til dobbelt så stor volumen ved konstant temperatur, gør trykket hvad?
Dette skyldes Boyle's lov, der siger, at presset fra en gas er omvendt proportionalt med dens volumen ved en konstant temperatur.
Matematisk kan dette udtrykkes som:
P₁v₁ =p₂v₂
Hvor:
* P₁ =oprindeligt tryk
* V₁ =indledende bind
* P₂ =endelig pres
* V₂ =slutvolumen
Da volumen fordobles (v₂ =2V₁), skal trykket falde med halvdelen (p₂ =p₁/2) for at opretholde ligheden.
Sidste artikelHvad er en egenskab for både fast tilstand og flydende tilstand?
Næste artikelHvad er et stof, der fremskynder kemisk proces?
 Varme artikler
Varme artikler
-
 Ny katalysator forvandler forurenende stoffer til brændstofHaotian Wang, hvem vil slutte sig til Rice fakultetet senere i år, er hovedforfatter til en undersøgelse, der skal omdanne kuldioxid til kulilte og andre industrielle brændstoffer. Kredit:Jon Chase/Ha
Ny katalysator forvandler forurenende stoffer til brændstofHaotian Wang, hvem vil slutte sig til Rice fakultetet senere i år, er hovedforfatter til en undersøgelse, der skal omdanne kuldioxid til kulilte og andre industrielle brændstoffer. Kredit:Jon Chase/Ha -
 Papir eller plastik? Stiv vandtæt belægning til papir har til formål at reducere vores afhængigh…En klassisk origami-kran lavet af papir og belagt med Choetsu (venstre) og ubestrøget (højre). Når den er nedsænket i vand, holder den belagte papirkran sin form, mens den ubestrøede hurtigt mættes me
Papir eller plastik? Stiv vandtæt belægning til papir har til formål at reducere vores afhængigh…En klassisk origami-kran lavet af papir og belagt med Choetsu (venstre) og ubestrøget (højre). Når den er nedsænket i vand, holder den belagte papirkran sin form, mens den ubestrøede hurtigt mættes me -
 Første nogensinde in-situ måling af mekaniske egenskaber af hærdet cementmørtel på dybt havTil venstre:Måleapparat ved siden af cementmørtelprøve ved en vanddybde på ca. 3, 500 meter. Til højre:Fjernbetjent køretøj ROV Kaiko Mk-IV, bruges til at installere cementmørtelprøven. Kredit:JAMST
Første nogensinde in-situ måling af mekaniske egenskaber af hærdet cementmørtel på dybt havTil venstre:Måleapparat ved siden af cementmørtelprøve ved en vanddybde på ca. 3, 500 meter. Til højre:Fjernbetjent køretøj ROV Kaiko Mk-IV, bruges til at installere cementmørtelprøven. Kredit:JAMST -
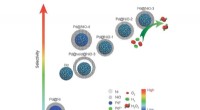 Interface engineering core@shell nanopartikler til aktiv og selektiv direkte H2O2-genereringSkematisk illustration, der viser aktiviteten og selektiviteten over for H2O2-syntese af 5 vægt% Pd@Ni-3/TiO2, 5 vægt% Pd@NiO-x/TiO2 (x =1, 2, 3, 4), 5 vægt% Pd@void@Ni-3/TiO2 og 5 vægt% Pd/Ti02. Kred
Interface engineering core@shell nanopartikler til aktiv og selektiv direkte H2O2-genereringSkematisk illustration, der viser aktiviteten og selektiviteten over for H2O2-syntese af 5 vægt% Pd@Ni-3/TiO2, 5 vægt% Pd@NiO-x/TiO2 (x =1, 2, 3, 4), 5 vægt% Pd@void@Ni-3/TiO2 og 5 vægt% Pd/Ti02. Kred
- Ny forskning transformerer glukosetransportproteiner til vandopløselig form
- Hvad ville der ske, hvis jorden pludselig var mere massiv end sol?
- Hvor meget energi bruger en delfin på at svømme?
- Affaldsproblem ved Englands beskyttede kyster
- De fleste ioniske forbindelser består af en?
- Hvor grundvand danner huler?


