Hvad er den effektive atomladning for en elektron i det yderste skal af et fluoratom F?
1. Forstå effektiv atomafgift
Effektiv atomafgift er den nettopositive ladning, der opleves af et elektron i et atom. Det er mindre end den faktiske atomafgift (antallet af protoner) på grund af afskærmningseffekten af indre elektroner.
2. Bestem atomantallet af fluor
Fluor (F) har et atomnummer på 9, hvilket betyder, at det har 9 protoner.
3. Bestem elektronkonfigurationen af fluor
Fluorens elektronkonfiguration er 1S² 2s² 2p⁵. Dette betyder, at det har:
* 2 elektroner i 1S -skallen
* 2 elektroner i 2S -skallen
* 5 elektroner i 2p -skallen
4. Beregn afskærmningskonstanten (r)
Afskærmningskonstanten (er) repræsenterer mængden af afskærmning leveret af de indre elektroner. En god tilnærmelse til afskærmningskonstanten er:
* kerneelektroner: Hver kerneelektron bidrager ca. 0,35 til afskærmningskonstanten.
* Elektroner i samme skal: Elektroner i samme skal bidrager ca. 0,35 til afskærmningskonstanten.
* Elektroner i underskaller med højere princip kvantenumre: Disse bidrager kun lidt til afskærmningskonstanten.
For fluor kan afskærmningskonstanten (r) estimeres som:
* 2 Elektroner i 1S -skallen:2 * 0,35 =0,7
* 2 Elektroner i 2S -skallen:2 * 0,35 =0,7
* 4 Elektroner i 2p -skallen:4 * 0,35 =1,4
Total afskærmningskonstant (r) =0,7 + 0,7 + 1,4 =2,8
5. Beregn effektiv nuklearafgift (ZEFF)
Zeff =Z (faktisk atomafgift) - S (afskærmningskonstant)
Zeff =9 - 2.8 = 6.2
Derfor er den effektive atomladning, der opleves af et elektron i den yderste skal af et fluoratom, cirka 6,2.
Sidste artikelHvad dannes, når et atom mister elektron til et andet atom?
Næste artikelAnklagen for subatomære partikler som proton?
 Varme artikler
Varme artikler
-
 Antistof mod kræftfremkaldende stof dechifreretNår fedt reagerer med glødende kul ved en grill, der dannes et stof, som kemikerne kalder benzopyren. Det er et udbredt miljøgift, der kan forårsage kræft hos mennesker. Kredit:Fotolia/Dederer Som
Antistof mod kræftfremkaldende stof dechifreretNår fedt reagerer med glødende kul ved en grill, der dannes et stof, som kemikerne kalder benzopyren. Det er et udbredt miljøgift, der kan forårsage kræft hos mennesker. Kredit:Fotolia/Dederer Som -
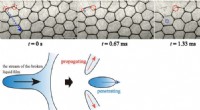 To distinkte fysiske mekanismer identificeret for, hvordan simple skum kollapserFilmen ses at trække sig tilbage i omgivende film, mens en dråbe frigives, som trænger ind i andre film og forårsager yderligere kollaps. Kredit:Rei Kurita Forskere fra Tokyo Metropolitan Universi
To distinkte fysiske mekanismer identificeret for, hvordan simple skum kollapserFilmen ses at trække sig tilbage i omgivende film, mens en dråbe frigives, som trænger ind i andre film og forårsager yderligere kollaps. Kredit:Rei Kurita Forskere fra Tokyo Metropolitan Universi -
 AI identificerer ændringer i mikrostruktur i aldrende materialerTopologisk analyse af røntgen-CT-data til genkendelse og trending af ændringer i mikrostruktur under materialeældning. Kredit:Lawrence Livermore National Laboratory Lawrence Livermore National Lab
AI identificerer ændringer i mikrostruktur i aldrende materialerTopologisk analyse af røntgen-CT-data til genkendelse og trending af ændringer i mikrostruktur under materialeældning. Kredit:Lawrence Livermore National Laboratory Lawrence Livermore National Lab -
 Fremstilling af bæredygtige polymerer fra duftende molekylerKredit:CC0 Public Domain En måde at fremstille organiske polymerer på fra de duftende molekyler i nåletræer og frugttræer er blevet udviklet af forskere ved University of Birmingham. Teknikken, u
Fremstilling af bæredygtige polymerer fra duftende molekylerKredit:CC0 Public Domain En måde at fremstille organiske polymerer på fra de duftende molekyler i nåletræer og frugttræer er blevet udviklet af forskere ved University of Birmingham. Teknikken, u
- Brændte træer og milliarder i kontanter:Hvordan et klimaprogram i Californien lader virksomheder b…
- Forskellen mellem elektrostatiske og magnetostatiske felter?
- Vil du løse verdens problemer? Prøv at arbejde sammen på tværs af discipliner
- Hvornår blev hastighed opdaget?
- Skjult liv afsløret inde i dinosaurknogler
- Bogen beskriver, hvordan den føderale regering brugte bestikkelse til at afslutte forholdet til ind…


