Når der leveres varme til et fast stof?
1. Stigning i temperatur:
* Den mest øjeblikkelige virkning er en stigning i den gennemsnitlige kinetiske energi af molekylerne inden for det faste stof. Denne øgede kinetiske energi får molekylerne til at vibrere mere kraftigt.
* Når temperaturen stiger, vibrerer molekylerne med større amplitude, men de forbliver i en fast, stiv struktur. Dette er den fase, hvor det faste stof stadig er i sin faste tilstand.
2. Ændring af tilstand (smeltning):
* Hvis der leveres nok varme, kan molekylernes kinetiske energi overvinde kræfterne, der holder dem i en fast struktur.
* Dette fører til en ændring af tilstand fra fast stof til væske, kendt som smeltning.
* Under smeltning forbliver temperaturen konstant, selvom der tilsættes varme. Dette skyldes, at energien bruges til at bryde de intermolekylære bindinger i stedet for at øge molekylernes kinetiske energi.
3. Yderligere stigning i temperatur:
* Når stoffet er smeltet, kan den flydende tilstand opvarmes yderligere, hvilket øger den gennemsnitlige kinetiske energi for molekylerne.
* De flydende molekyler er frie til at bevæge sig rundt, men de forbliver stadig i nærheden af hinanden.
4. Ændring af tilstand (kogning/fordampning):
* Hvis der leveres nok varme til væsken, kan molekylerne få nok kinetisk energi til at overvinde kræfterne, der holder dem sammen helt.
* Dette fører til en ændring af tilstand fra væske til gas, kendt som kogning eller fordampning.
* I lighed med smeltning forbliver temperaturen konstant under kogning, mens varmen bruges til at bryde de intermolekylære kræfter.
5. Yderligere stigning i temperatur:
* Når stoffet er fordampet, kan gastilstanden opvarmes yderligere, hvilket øger den gennemsnitlige kinetiske energi for molekylerne.
* Gasmolekylerne er frie til at bevæge sig rundt og er langt fra hinanden.
Andre faktorer:
* Mængden af varme, der kræves for at forårsage en tilstandsændring, afhænger af den specifikke varmekapacitet af stoffet.
* Forskellige stoffer har forskellige smeltnings- og kogepunkter, hvilket indikerer den mængde energi, der kræves for at ændre deres tilstand.
* Trykket omkring stoffet kan også påvirke dets smelte- og kogepunkter.
Sammenfattende kan levering af varme til et fast stof forårsage en stigning i temperatur, en tilstandsskift til væske og derefter gas eller begge dele, afhængigt af mængden af varme og stoffets egenskaber.
Sidste artikelDe fleste halogener danner forbindelser af hvad?
Næste artikelHvad er elektronarrangementet for ilt?
 Varme artikler
Varme artikler
-
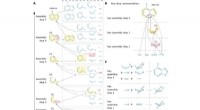 Samlingsteori kan betyde gode nyheder for lægemiddelopdagelseFig. 1. Repræsentationer af en samlingsvej, ved at tage adenin som eksempel. (A) En af adenins mange samlingsveje (det viser sig at være den korteste, ifølge vores MC-algoritme, forklaret senere). Sam
Samlingsteori kan betyde gode nyheder for lægemiddelopdagelseFig. 1. Repræsentationer af en samlingsvej, ved at tage adenin som eksempel. (A) En af adenins mange samlingsveje (det viser sig at være den korteste, ifølge vores MC-algoritme, forklaret senere). Sam -
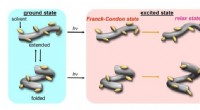 Under tryk:Manipulering af protein-efterlignende molekyler med hydrostatisk trykI grundtilstanden, værten vedtager to konformere, en forlænget og en foldet, og gradvist skifter til en udvidet-rig tilstand efter tryk. Derefter, i ophidset tilstand (hυ), disse to konformere udsende
Under tryk:Manipulering af protein-efterlignende molekyler med hydrostatisk trykI grundtilstanden, værten vedtager to konformere, en forlænget og en foldet, og gradvist skifter til en udvidet-rig tilstand efter tryk. Derefter, i ophidset tilstand (hυ), disse to konformere udsende -
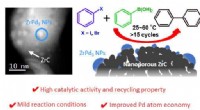 En kombineret strategi i katalysatordesign til Suzuki krydskoblingerOversigt over den nye Pd-ZrC heterogene katalysator. Den nye katalysator består af ZrPd3-nanopartikler dyrket på en inert ZrC-understøtning. Dens enkle fremstillingsprocedure, kombineret med dets mang
En kombineret strategi i katalysatordesign til Suzuki krydskoblingerOversigt over den nye Pd-ZrC heterogene katalysator. Den nye katalysator består af ZrPd3-nanopartikler dyrket på en inert ZrC-understøtning. Dens enkle fremstillingsprocedure, kombineret med dets mang -
 Indfanger adfærden af enkeltatom-katalysatorer på fartenEn ny undersøgelse kontrollerede præcist fastgørelsen af platinatomer (hvide kugler) til en titaniumdioxidoverflade (gitterværk af røde og blå kugler). Den fandt, at deres positioner varierede fra a
Indfanger adfærden af enkeltatom-katalysatorer på fartenEn ny undersøgelse kontrollerede præcist fastgørelsen af platinatomer (hvide kugler) til en titaniumdioxidoverflade (gitterværk af røde og blå kugler). Den fandt, at deres positioner varierede fra a
- Hvordan finder man en stjernehob? Let, tæl simpelthen stjernerne
- Elbilmarkedet sætter gang i koboltpriserne
- Rocket fungerer efter princippet om bevarelse af?
- Hvilke lande spiser mest energi?
- Hvad er en fluid -model inden for elektricitet?
- Hvad kaldes et stof, der er dannet som et resultat af kemisk reaktion?


