Hvad er Bohr Atom -modellen af kalium?
1. Nucleus:
* Kalium (K) har et atomnummer på 19, hvilket betyder, at det har 19 protoner i sin kerne.
* Det har også 20 neutroner (i sin mest almindelige isotop, kalium-39).
2. Elektronskaller:
* shell 1 (k shell): Indeholder 2 elektroner.
* shell 2 (l shell): Indeholder 8 elektroner.
* shell 3 (m shell): Indeholder 8 elektroner.
* shell 4 (n shell): Indeholder 1 elektron.
diagram:
Du kan visualisere dette som koncentriske cirkler omkring kernen, med den første cirkel (k shell) tættest på kernen og den fjerde cirkel (n shell) længst. Hver cirkel har et specifikt antal elektroner.
Vigtige overvejelser:
* Bohr -modellen er ikke helt nøjagtig. Det afbilder ikke den faktiske bølgelignende karakter af elektroner eller sandsynligheden for at finde dem i en bestemt region.
* Valenselektronen: Kaliums enkelte elektron i den yderste skal (N shell) er dens valenselektron. Dette er det elektron, der deltager i kemisk binding.
* reaktivitet: På grund af sin enkelt valenselektron er kalium meget reaktiv og danner let en +1 -kation ved at miste denne elektron.
Moderne atomteori:
Mens BoHR -modellen er et nyttigt værktøj, er det vigtigt at huske, at moderne atomteori beskriver elektroner som besættende orbitaler, som er regioner af sandsynlighed snarere end faste kredsløb.
Sidste artikelHvad gør et materiale til bedre leder end et andet?
Næste artikelHvad er et stof, der ikke leder?
 Varme artikler
Varme artikler
-
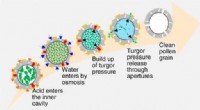 Rensning af pollenskallerKredit:American Chemical Society Efterhånden som allergisæsonen intensiveres, mange mennesker forbander pollen - det pulveragtige stof, der frigives af planter til reproduktion. Imidlertid, pollen
Rensning af pollenskallerKredit:American Chemical Society Efterhånden som allergisæsonen intensiveres, mange mennesker forbander pollen - det pulveragtige stof, der frigives af planter til reproduktion. Imidlertid, pollen -
 Lysfarvet 3D-print ved hjælp af flydende krystallera) Oversigt over det centrale element i direkte blækskrivning (DIW):sprøjten med mikrodyse. Angivet er placeringen af blækket, varmekappen (til temperaturstyret DIW), mikrodysen og det trykte objekt
Lysfarvet 3D-print ved hjælp af flydende krystallera) Oversigt over det centrale element i direkte blækskrivning (DIW):sprøjten med mikrodyse. Angivet er placeringen af blækket, varmekappen (til temperaturstyret DIW), mikrodysen og det trykte objekt -
 Infrarød sensor som ny metode til opdagelse af lægemidlerDen infrarøde sensor blev udviklet af Klaus Gerwert (til venstre) og Jörn Güldenhaupt. Kredit:Gerd Kock Ved hjælp af en infrarød sensor, biofysikere ved Ruhr-Universität Bochum (RUB) er lykkedes h
Infrarød sensor som ny metode til opdagelse af lægemidlerDen infrarøde sensor blev udviklet af Klaus Gerwert (til venstre) og Jörn Güldenhaupt. Kredit:Gerd Kock Ved hjælp af en infrarød sensor, biofysikere ved Ruhr-Universität Bochum (RUB) er lykkedes h -
 En ny polyethylen-B4C baseret beton til afskærmningKredit:ESS/SINE2020 Afskærmning spiller en vigtig rolle ved neutronkilder for både strålingssikkerhed og for at minimere baggrundsstøj i neutronforsøg. Afskærmning er regelmæssigt lavet af beton,
En ny polyethylen-B4C baseret beton til afskærmningKredit:ESS/SINE2020 Afskærmning spiller en vigtig rolle ved neutronkilder for både strålingssikkerhed og for at minimere baggrundsstøj i neutronforsøg. Afskærmning er regelmæssigt lavet af beton,
- Lavprotein kost i det tidlige liv øger levetiden hos frugtfluer
- Sort boligejerskab er det laveste siden 1968; hvad det betyder i et valgår
- Hvilket elektromagnetisk spektrum er energi, der bevæger sig med stråling?
- Hvad tid åbner Air and Space Museum i Washington D.C.?
- Hvordan ville en organisme sandsynligvis blive påvirket af en DNA -mutation?
- En skov af nanosvampestrukturer holder denne plast ren og pletfri


