Hvad er forholdet mellem tæthed og specifik varmekapacitet af et rent stof?
Her er hvorfor:
* densitet er et mål for, hvor meget masse der er indeholdt i et givet volumen. Det bestemmes af arrangementet og pakningen af molekyler i et stof.
* Specifik varmekapacitet er et mål for, hvor meget varmeenergi der kræves for at hæve temperaturen på en enhedsmasse af et stof i en grad. Det bestemmes af molekylstrukturen og typerne af bindinger i stoffet.
Eksempler:
* vand Har en relativt høj specifik varmekapacitet, hvilket betyder, at det kræver en masse energi at hæve temperaturen. Vand har imidlertid en ret høj densitet.
* aluminium Har en lav specifik varmekapacitet, hvilket betyder, at den opvarmes hurtigt. Det har også en lavere tæthed end vand.
faktorer, der påvirker specifik varmekapacitet:
* Intermolekylære kræfter: Stærkere intermolekylære kræfter kræver mere energi til at bryde, hvilket resulterer i en højere specifik varmekapacitet.
* molekylær kompleksitet: Mere komplekse molekyler har flere vibrationsmetoder, hvilket kræver mere energi for at hæve deres temperatur.
* fase af stof: Faststoffer har generelt lavere specifikke varmekapaciteter end væsker, der har lavere specifikke varmekapacitet end gasser.
Kortfattet:
Densitet og specifik varmekapacitet er forskellige egenskaber ved et stof og er ikke direkte relateret. De er påvirket af forskellige faktorer og har forskellige konsekvenser for materialernes opførsel.
 Varme artikler
Varme artikler
-
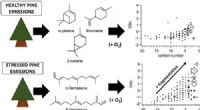 Bladlusstressede fyrretræer viser forskellig sekundær organisk aerosoldannelseKredit:American Chemical Society Planter udsender gasser, kaldet flygtige organiske forbindelser (VOCer), der kommer ind i atmosfæren, hvor de kan interagere med andre naturlige og menneskeskabte
Bladlusstressede fyrretræer viser forskellig sekundær organisk aerosoldannelseKredit:American Chemical Society Planter udsender gasser, kaldet flygtige organiske forbindelser (VOCer), der kommer ind i atmosfæren, hvor de kan interagere med andre naturlige og menneskeskabte -
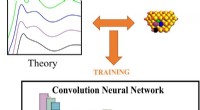 Maskinlæringsanalyse af røntgendata udvælger vigtige katalytiske egenskaberDette skema viser, hvordan spektre afledt af teoriberegninger ved hjælp af kendte strukturer (øverst) kan bruges til at træne et neuralt netværk (i midten), som så kan bruge sin samlede viden til at o
Maskinlæringsanalyse af røntgendata udvælger vigtige katalytiske egenskaberDette skema viser, hvordan spektre afledt af teoriberegninger ved hjælp af kendte strukturer (øverst) kan bruges til at træne et neuralt netværk (i midten), som så kan bruge sin samlede viden til at o -
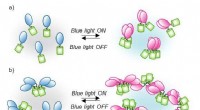 Proteinblanding under blåt lysSkema af CRY2PHR klyngemekanismen udløst af blåt lys. I dette optogenetiske system, CRY2-klynger (blå og pink) styres reversibelt af blåt lys. Hvis CRY2 er forbundet med fluorescerende proteiner (grøn
Proteinblanding under blåt lysSkema af CRY2PHR klyngemekanismen udløst af blåt lys. I dette optogenetiske system, CRY2-klynger (blå og pink) styres reversibelt af blåt lys. Hvis CRY2 er forbundet med fluorescerende proteiner (grøn -
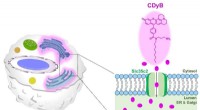 En enklere måde at differentiere B-celler og T-celler påDen foreslåede farvningsmekanisme af CDyB. Kredit:Institut for Grundvidenskab Vores immunsystem er afgørende for vores overlevelse, da vores kroppe konstant bliver udsat for bakterier, vira, parasi
En enklere måde at differentiere B-celler og T-celler påDen foreslåede farvningsmekanisme af CDyB. Kredit:Institut for Grundvidenskab Vores immunsystem er afgørende for vores overlevelse, da vores kroppe konstant bliver udsat for bakterier, vira, parasi
- Eksperter søger svar bag konstante jordskælv i Puerto Rico
- Hvor mange kilo er der i et mikrogram?
- Hvor mange molekyler i alt har NF3 omkring det centrale atom?
- Vask dine hænder i 20 sekunder:Fysikken viser hvorfor
- Hvilken organelle konverterer sollys energi?
- Forskere forudsiger rekordstor orkansæson 2018


