Hvilken eksperimentel metode har gjort det muligt for forskere at estimere atomisk og ionisk radi?
1. Røntgenstrålediffraktion (XRD):
* hvordan det fungerer: Røntgenstrålediffraktion involverer skinnende røntgenstråler på en krystallinsk prøve. Atomerne i krystal diffracerer røntgenstrålerne, hvilket skaber et mønster af pletter på en detektor. Dette mønster kan analyseres for at bestemme arrangementet af atomer i krystallen, inklusive afstandene mellem dem.
* Begrænsninger: XRD giver kun information om afstanden mellem atomer i en fast tilstand. Det måler ikke direkte størrelsen på individuelle atomer.
2. Elektrondiffraktion:
* hvordan det fungerer: I lighed med XRD bruger elektrondiffraktion en stråle af elektroner til at undersøge materialernes struktur. Elektroner interagerer med atomernes elektronskyer, hvilket giver information om fordelingen af elektroner og størrelsen på atomet.
* Begrænsninger: Elektrondiffraktion er mere følsom over for overfladen af et materiale og er muligvis ikke så præcis til bestemmelse af atomradier som andre metoder.
3. Teoretiske beregninger:
* hvordan det fungerer: Kvantemekaniske beregninger kan bruges til at modellere opførsel af elektroner i atomer og molekyler. Disse beregninger kan tilvejebringe estimater af størrelserne af atomer og ioner baseret på fordelingen af elektrondensitet.
* Begrænsninger: Nøjagtigheden af disse beregninger afhænger af kompleksiteten af det system, der er modelleret og de anvendte tilnærmelser.
4. Empiriske tendenser:
* hvordan det fungerer: Forskere har observeret tendenser inden for atom- og ionisk radier på tværs af den periodiske tabel. For eksempel falder atomradius generelt i en periode og øges ned ad en gruppe. Disse tendenser kan bruges til at estimere størrelsen på et atom eller ion baseret på dets position i den periodiske tabel.
* Begrænsninger: Empiriske tendenser er baseret på generaliseringer og er muligvis ikke nøjagtige for alle elementer eller ioner.
Bestemmelse af ioniske radier:
* Ioniske radier bestemmes ved at analysere afstandene mellem ioner i ioniske krystaller.
* Røntgenstrålediffraktion er den primære teknik, der bruges til at måle disse afstande.
* Den ioniske radius beregnes ved at trække radius for den anden ion fra afstanden mellem dem.
Vigtige overvejelser:
* Atomiske og ioniske radier er ikke faste værdier. De kan variere afhængigt af det kemiske miljø i atomet eller ion.
* De metoder, der bruges til at estimere disse værdier, har iboende begrænsninger og usikkerheder.
* De rapporterede værdier for atomiske og ioniske radier er normalt gennemsnit opnået fra forskellige eksperimentelle og teoretiske metoder.
Sammenfattende er der ingen enkelt "guldstandard" -metode til bestemmelse af atomisk og ionisk radier. Forskere bruger en kombination af eksperimentelle teknikker, teoretiske beregninger og empiriske tendenser til at estimere disse værdier, der anerkender begrænsningerne i hver metode.
 Varme artikler
Varme artikler
-
 Forskerhold skruer op for varmen på 3D-printblækEn 3D-printet blomst demonstrerer kvaliteterne af en multifunktionel printgel, der reagerer på fugt. Kredit:Ke Functional Research Group i Dartmouth. En proces, der bruger varme til at ændre arran
Forskerhold skruer op for varmen på 3D-printblækEn 3D-printet blomst demonstrerer kvaliteterne af en multifunktionel printgel, der reagerer på fugt. Kredit:Ke Functional Research Group i Dartmouth. En proces, der bruger varme til at ændre arran -
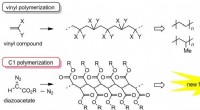 Udvikling af en ny slutfunktionaliseringsteknik i polymersyntesePolymerisation af vinylforbindelse og C1-polymerisation af diazoacetat. Kredit:Ehime University Vinylpolymerisation (polymerisation af vinylforbindelser) er en nyttig metode til fremstilling af sp3
Udvikling af en ny slutfunktionaliseringsteknik i polymersyntesePolymerisation af vinylforbindelse og C1-polymerisation af diazoacetat. Kredit:Ehime University Vinylpolymerisation (polymerisation af vinylforbindelser) er en nyttig metode til fremstilling af sp3 -
 Enkeltmolekyle påvisning af kræftmarkører bringer flydende biopsi tættere på klinikkenHver prik, der ses på dette PRAM-billede, repræsenterer ét mikroRNA, der er bundet til sensoren. Kredit:Nantao Li En hurtig, billig, men følsom teknik til at opdage kræftmarkører bringer forskere
Enkeltmolekyle påvisning af kræftmarkører bringer flydende biopsi tættere på klinikkenHver prik, der ses på dette PRAM-billede, repræsenterer ét mikroRNA, der er bundet til sensoren. Kredit:Nantao Li En hurtig, billig, men følsom teknik til at opdage kræftmarkører bringer forskere -
 Palladiumkatalysator fremskynder to separate reaktioner, fremstilling af nyttige molekyler i en enke…Pterostilbene (billedet), et defensivt kemikalie fundet i blåbær, er et eksempel på et funktionelt molekyle, der indeholder stilben-motivet. Kredit:MOLEKUUL/SCIENCE PHOTO LIBRARY En palladiumkatal
Palladiumkatalysator fremskynder to separate reaktioner, fremstilling af nyttige molekyler i en enke…Pterostilbene (billedet), et defensivt kemikalie fundet i blåbær, er et eksempel på et funktionelt molekyle, der indeholder stilben-motivet. Kredit:MOLEKUUL/SCIENCE PHOTO LIBRARY En palladiumkatal
- Klimaforandringerne viser sig i krympende sne i Antarktis
- Mennesker med handicap bærer den største belastning af græstørvskampe mellem konventionelle og o…
- Hvilket objekt har lav kinetisk energi?
- Hvad gør kviksølv unik sammenlignet med andre planeter i vores solsystem?
- Brand i Californien aflyser cykeltur, opfordrer til evakueringer
- Hvor meget arbejde udføres af en styrke på 60 N, der bevæger et objekt 6 meter?


