Er saltvand en isolator eller en leder?
* opløste ioner: Når salt (natriumchlorid, NaCl) opløses i vand, opdeles det i positivt ladede natriumioner (Na+) og negativt ladede chloridioner (CL-). Disse ioner er frie til at bevæge sig inden i vandet og skabe en vej til elektrisk strøm.
* elektrolyt: Opløsninger som saltvand, der indeholder frie ioner, kaldes elektrolytter. Elektrolytter udfører elektricitet, fordi ionerne kan bære den elektriske ladning.
* Konduktivitet varierer: Konduktiviteten af saltvand afhænger af koncentrationen af salt. Jo mere salt opløst, jo flere ioner er til stede, og jo bedre ledningsevne.
I modsætning hertil er rent vand en meget dårlig leder af elektricitet. Dette skyldes, at rent vand indeholder meget få frie ioner.
Vigtig note: Selv lidt salt vand kan være farligt. Håndter aldrig elektrisk udstyr eller apparater med våde hænder, især hvis vandet indeholder salt.
 Varme artikler
Varme artikler
-
 Ny teori for, hvordan snefnug vokserKredit:Pixabay/CC0 Public Domain Forskere har opdaget, hvad der driver det sarte og komplekse mikrokosmos af små terrasser, pyramider og kratere fundet på overfladen af is. Disse miniature struk
Ny teori for, hvordan snefnug vokserKredit:Pixabay/CC0 Public Domain Forskere har opdaget, hvad der driver det sarte og komplekse mikrokosmos af små terrasser, pyramider og kratere fundet på overfladen af is. Disse miniature struk -
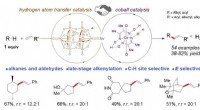 Ny metode til funktionalisering af carbon-hydrogen-bindinger i de sene stadierIllustration, der viser (øverst) den stedselektive C-H-alkenylering i det sene trin ved brug af synergistisk hydrogenatomoverførsel og koboltkatalyse i nærvær af lys (hv). (Bund) Udvalg af kemiske pro
Ny metode til funktionalisering af carbon-hydrogen-bindinger i de sene stadierIllustration, der viser (øverst) den stedselektive C-H-alkenylering i det sene trin ved brug af synergistisk hydrogenatomoverførsel og koboltkatalyse i nærvær af lys (hv). (Bund) Udvalg af kemiske pro -
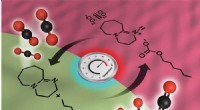 Forskere bekræfter forskellige regioner i populært kulstoffangst og syntese opløsningsmiddelBagsiden af Physical Chemistry Chemical Physics viser et stiliseret billede af de forskellige regioner i SWIL, og hvordan kuldioxiden bevæger sig mellem regionerne baseret på temperatur. Kredit:Mike
Forskere bekræfter forskellige regioner i populært kulstoffangst og syntese opløsningsmiddelBagsiden af Physical Chemistry Chemical Physics viser et stiliseret billede af de forskellige regioner i SWIL, og hvordan kuldioxiden bevæger sig mellem regionerne baseret på temperatur. Kredit:Mike -
 Polymerer kan reducere skader forårsaget af lossepladserKredit:CC0 Public Domain En bachelor-forsker fra Binghamton University håber at reducere påvirkningen af lossepladser på miljøet. Eleonora Recio, en junior hovedfag i maskinteknik med et bifag
Polymerer kan reducere skader forårsaget af lossepladserKredit:CC0 Public Domain En bachelor-forsker fra Binghamton University håber at reducere påvirkningen af lossepladser på miljøet. Eleonora Recio, en junior hovedfag i maskinteknik med et bifag
- Dawn-missionen til asteroidebæltet slutter
- Hvad er reglerne for fysikspil magisk pen?
- Hvor mange ækvivalenter af Mg plus 2 er til stede i en opløsning, der indeholder 2,75 mol 2?
- Typer af ting, der bruger atomenergi?
- Hvad er faktisk stråling?
- Hvad er den effektive atomladning for en elektron i det yderste skal af et fluoratom F?


