Hvad øges i volumenet af et stof, når temperaturen øges?
Her er en mere detaljeret forklaring:
* faste stoffer: Molekylerne i faste stoffer er tæt pakket og vibrerer på plads. Når temperaturen stiger, bliver vibrationerne mere intense, hvilket får molekylerne til at bevæge sig lidt længere fra hinanden, hvilket fører til en lille stigning i volumen.
* væsker: Væsker har mere bevægelsesfrihed end faste stoffer. Når temperaturen stiger, bevæger molekylerne sig hurtigere og længere fra hinanden, hvilket resulterer i en mere markant stigning i volumen sammenlignet med faste stoffer.
* Gasser: Gasser er meget komprimerbare og har meget større afstande mellem molekyler. Når de opvarmes, bevæger gasmolekyler sig meget hurtigere, hvilket fører til en meget stor stigning i volumen.
Undtagelser:
* Vand: Vand er en undtagelse fra denne generelle regel. Mellem 0 ° C og 4 ° C falder vandmængden faktisk *, når temperaturen stiger. Dette skyldes den unikke struktur af vandmolekyler, som giver dem mulighed for at danne hydrogenbindinger.
* Andre stoffer: Der er et par andre stoffer, især nogle metaller, der udviser lignende opførsel som vand over et lille temperaturområde.
Key Takeaway:
Stigningen i volumen på grund af temperaturændringer kaldes generelt termisk ekspansion . Dette princip bruges i forskellige applikationer, såsom termometre, bimetalliske strimler og ingeniørdesign, der tegner sig for ændringer i materialer på grund af temperaturvariationer.
Sidste artikelFlytter molekyle hurtigere ved høje eller lave temperaturer?
Næste artikelKan væsker og faststof komprimeres?
 Varme artikler
Varme artikler
-
 Forskere forstår endelig enzymernes arbejdsugeKredit:Københavns Universitet Enzymer bruges meget i vores hverdag. Som små soldater, enzymer i vaskepulver arbejder for at fjerne fedtpletter fra tøj, ligesom de bruges til at omdanne halm til bi
Forskere forstår endelig enzymernes arbejdsugeKredit:Københavns Universitet Enzymer bruges meget i vores hverdag. Som små soldater, enzymer i vaskepulver arbejder for at fjerne fedtpletter fra tøj, ligesom de bruges til at omdanne halm til bi -
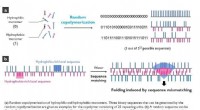 Ny polymer mesofasestruktur opdagetKredit:Korea Advanced Institute of Science and Technology Polymerer, store molekyler, der består af gentagne mindre molekyler kaldet monomerer, findes i næsten alt, hvad vi bruger i vores daglige l
Ny polymer mesofasestruktur opdagetKredit:Korea Advanced Institute of Science and Technology Polymerer, store molekyler, der består af gentagne mindre molekyler kaldet monomerer, findes i næsten alt, hvad vi bruger i vores daglige l -
 Hvordan blækspruttecamouflage kan hjælpe med at forhindre hudkræft hos menneskerEt team af nordøstlige forskere bruger kemien i blækspruttehud til at skabe en bærbar enhed, der registrerer skadelige niveauer af UV-stråling. Kredit:Alyssa Stone/Northeastern University Det var i
Hvordan blækspruttecamouflage kan hjælpe med at forhindre hudkræft hos menneskerEt team af nordøstlige forskere bruger kemien i blækspruttehud til at skabe en bærbar enhed, der registrerer skadelige niveauer af UV-stråling. Kredit:Alyssa Stone/Northeastern University Det var i -
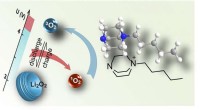 Batteriforskning:nye gennembrud inden for forskning i superbatterierDannelsen af singlet oxygen (1O2) forringer cyklusstabiliteten af mange alkalimetalkatoder, såsom Li-O2 katoden. I tidsskriftet præsenterer Angewandte Chemie Freunberger en effektiv og højspænding
Batteriforskning:nye gennembrud inden for forskning i superbatterierDannelsen af singlet oxygen (1O2) forringer cyklusstabiliteten af mange alkalimetalkatoder, såsom Li-O2 katoden. I tidsskriftet præsenterer Angewandte Chemie Freunberger en effektiv og højspænding


