Hvorfor absorberes kortere bølgelængder i gasmolekyler snarere end lange bølgelængder?
* Energiniveau: Molekyler har specifikke energiniveauer. Når en foton interagerer med et molekyle, skal fotons energi matche forskellen mellem to energiniveauer for at absorption kan forekomme. Kortere bølgelængder bærer mere energi end længere bølgelængder (tænk på forholdet mellem frekvens og energi:e =hν, hvor e er energi, h er plancks konstante, og v er frekvens). Derfor er det mere sandsynligt, at kortere bølgelængder har den rigtige mængde energi til at begejstre et molekyle til et højere energiniveau.
* resonans: Begrebet resonans er vigtigt her. Ligesom en tuninggaffel vibrerer, når den udsættes for dens resonansfrekvens, vil et molekyle "resonere" med elektromagnetisk stråling, hvis frekvens matcher forskellen mellem dens energiniveau. Denne resonans fører til absorption af fotons energi.
* molekylære vibrationer og rotationer: Molekyler er ikke statiske enheder; De vibrerer og roterer. Disse vibrationer og rotationer svarer til specifikke energiniveauer. Kortere bølgelængder har den rigtige energi til at forårsage disse vibrationer og rotationer, hvilket øger sandsynligheden for absorption.
Tænk på det sådan:
* Forestil dig en sving. Du kan skubbe den forsigtigt med en lang bølgelængde (lav energi), og det svajer muligvis lidt.
* Men hvis du skubber den med en kort bølgelængde (høj energi), er det mere sandsynligt, at du får en stor sving og overfører din energi til gyngen.
Vigtige noter:
* Ikke alle molekyler absorberer alle korte bølgelængder: De specifikke bølgelængder, der absorberes, afhænger af molekylets struktur og dens energiniveauforskelle.
* længere bølgelængder kan stadig absorberes: Selvom mindre almindelige, kan længere bølgelængder absorberes, hvis energiforskellen mellem energiniveauet er tilstrækkelig lille.
Fortæl mig, hvis du har andre spørgsmål!
Sidste artikelHvad er fordampning, der forekommer på overfladen af en væske?
Næste artikelHvad er neutrale pioner lavet af?
 Varme artikler
Varme artikler
-
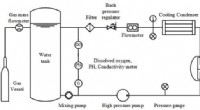 Forskere opnår nye resultater om korrosionsadfærd af legeringsmaterialer under ekstreme miljøerFig. 1. Skematisk diagram af højtemperatur- og højtryksvanddynamisk korrosionsanordning. Kredit:LIU Chao Materialers serviceadfærd under ekstreme miljøer er en af flaskehalsene, der begrænser ud
Forskere opnår nye resultater om korrosionsadfærd af legeringsmaterialer under ekstreme miljøerFig. 1. Skematisk diagram af højtemperatur- og højtryksvanddynamisk korrosionsanordning. Kredit:LIU Chao Materialers serviceadfærd under ekstreme miljøer er en af flaskehalsene, der begrænser ud -
 Beregningsmæssig forskning beskriver aktiveringsmekanismen for p38-alfaForskere afslørede detaljer om p38 -aktiveringsmekanismen. Billedet repræsenterer de strukturelle ændringer fra den inaktive tilstand (lilla) til den aktive (grøn) foreslået af røntgenkrystallografi.
Beregningsmæssig forskning beskriver aktiveringsmekanismen for p38-alfaForskere afslørede detaljer om p38 -aktiveringsmekanismen. Billedet repræsenterer de strukturelle ændringer fra den inaktive tilstand (lilla) til den aktive (grøn) foreslået af røntgenkrystallografi. -
 Dette røde lys betyder, at gå efter medicinske opdagelserUVA’s Hui-wang Ai, Ph.d., og Shen Zhang, Ph.d., har udviklet en enkel og effektiv forbedring af fluorescerende biosensorer, der er meget udbredt inden for videnskabelig og medicinsk forskning. Kredit:
Dette røde lys betyder, at gå efter medicinske opdagelserUVA’s Hui-wang Ai, Ph.d., og Shen Zhang, Ph.d., har udviklet en enkel og effektiv forbedring af fluorescerende biosensorer, der er meget udbredt inden for videnskabelig og medicinsk forskning. Kredit: -
 Ny proces til konservering af tømmer kan give fordele i forhold til trykbehandlingBehandlede og ubehandlede tømmerstykker nedsænket i vand. Tømmeret til venstre er blevet behandlet ved hjælp af atomlagsaflejring. Det modstår at absorbere vand, selv når det er nedsænket. Til højre e
Ny proces til konservering af tømmer kan give fordele i forhold til trykbehandlingBehandlede og ubehandlede tømmerstykker nedsænket i vand. Tømmeret til venstre er blevet behandlet ved hjælp af atomlagsaflejring. Det modstår at absorbere vand, selv når det er nedsænket. Til højre e
- Forskere finjusterer systemet for at skabe syngas fra CO2
- Hvad er den vigtigste organisme i nitrogencyklus?
- Hvad er forskellen mellem kobberrige malme og lave malme?
- Hvad er pigmenternes rolle i fotosyntese?
- Californiske kondorer vender tilbage til himlen efter næsten udryddelse
- Hvad er karakteristisk for en kovalent binding?


