Hvorfor har pentan en højere densitet end 2-2-dimethylpropan?
Her er hvorfor:
* form og pakning: Pentane har en lineær eller let forgrenet struktur, hvilket betyder, at dens molekyler kan pakke tæt sammen. Dette fører til en højere densitet. 2,2-dimethylpropan har på den anden side en meget kompakt, sfærisk form på grund af forgreningen ved kulstofkæden. Denne sfæriske form forhindrer effektiv pakning, hvilket resulterer i en lavere densitet.
* Intermolekylære kræfter: Mens begge molekyler kun har London-spredningskræfter (svage intermolekylære kræfter), giver den mere kompakte struktur af 2,2-dimethylpropan mulighed for stærkere London-spredningskræfter på grund af et større overfladeareal for interaktion. Denne lidt højere intermolekylære kraft bidrager til en højere densitet.
Kortfattet:
* 2,2-dimethylpropan (Neopentane) har en højere densitet end pentan på grund af dens kompakte, sfæriske struktur, som giver mulighed for mere effektiv pakning og stærkere intermolekylære kræfter.
Fortæl mig, hvis du gerne vil have flere oplysninger om densitet eller intermolekylære kræfter!
Sidste artikelHvad videnskabsmand opdagede, at atomer har en positiv ladning?
Næste artikelHvordan er subatomære partikler arrangeret?
 Varme artikler
Varme artikler
-
 Forskere udvikler en ny kombineret proces til 3D-printInde i det 3-D-printede materiale (til højre) indeholder en gitterstruktur (til venstre) de tilsatte væsker. Kredit:Harald Rupp/Uni Halle Kemikere ved Martin Luther University Halle-Wittenberg (ML
Forskere udvikler en ny kombineret proces til 3D-printInde i det 3-D-printede materiale (til højre) indeholder en gitterstruktur (til venstre) de tilsatte væsker. Kredit:Harald Rupp/Uni Halle Kemikere ved Martin Luther University Halle-Wittenberg (ML -
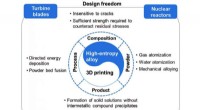 Forskere gennemgår fremskridt inden for 3D-print af højentropi-legeringerOversigt over forholdet mellem HEAer og 3D-print, med hensyn til kompositionsdesignet, pulver udvikling, trykprocesser, produkt egenskaber, og potentielle applikationer. Kredit:SUTD Højentropi-leg
Forskere gennemgår fremskridt inden for 3D-print af højentropi-legeringerOversigt over forholdet mellem HEAer og 3D-print, med hensyn til kompositionsdesignet, pulver udvikling, trykprocesser, produkt egenskaber, og potentielle applikationer. Kredit:SUTD Højentropi-leg -
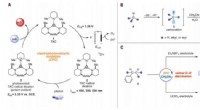 Elektrofotokatalytisk diamination af vicinale C -H -bindingerElektrofotokatalytisk amination af C -H -bindinger. (A) Generisk elektrofotokatalytisk cyklus med trisaminocyclopropenium (TAC) 1. (B) Ritter-type C-H amineringsreaktion. (C) Elektrofotokatalytiske vi
Elektrofotokatalytisk diamination af vicinale C -H -bindingerElektrofotokatalytisk amination af C -H -bindinger. (A) Generisk elektrofotokatalytisk cyklus med trisaminocyclopropenium (TAC) 1. (B) Ritter-type C-H amineringsreaktion. (C) Elektrofotokatalytiske vi -
 Ny katalytisk proces gør plastposer til limBrug af en katalysator baseret på ruthenium (guldkugle, centrum), UC Berkeley -kemikere var i stand til at tilføje specifikke kemiske grupper - i dette tilfælde, OH (rød) - til polyethylenpolymerkæder
Ny katalytisk proces gør plastposer til limBrug af en katalysator baseret på ruthenium (guldkugle, centrum), UC Berkeley -kemikere var i stand til at tilføje specifikke kemiske grupper - i dette tilfælde, OH (rød) - til polyethylenpolymerkæder
- Stærke vinde skaber australsk megablaze
- Hvordan bryder lava ud under vand?
- Forskere skræddersyr E. coli til at omdanne planter til vedvarende kemikalier
- Hvorfor der er en formørkelse hver 2. uge?
- Hvad er identitetsegenskaberne ved multiplikation?
- Forskere opnår gennembrud inden for højeffektiv elektrokatalysator til ren energi


