Med Bohr -effekten frigives mere ilt, fordi?
* CO2 og H+ binder til hæmoglobin: CO2 reagerer med vand i røde blodlegemer for at danne kulsyre (H2CO3), der adskiller sig til H+ og bicarbonat (HCO3-). Disse protoner (H+) binder til hæmoglobin og ændrer dens struktur.
* Strukturændring i hæmoglobin: Bindingen af H+ forårsager en konformationel ændring i hæmoglobinmolekylet. Denne ændring mindsker affiniteten af hæmoglobin for ilt, hvilket gør det lettere at frigive ilt i vævene.
* letter iltlevering: Dette fald i affinitet er afgørende for at levere ilt til væv, der er metabolisk aktive og producerer mere CO2 og H+, hvilket har en lavere pH. Disse væv kræver mere ilt.
I det væsentlige er Bohr -effekten en mekanisme, der hjælper med at sikre, at ilt leveres til de væv, der har mest brug for det.
Sidste artikelHvad er enheden for molekylært brydningsindeks?
Næste artikelHvordan opdagede Ernest Rutherford atomet?
 Varme artikler
Varme artikler
-
 Forskere opdager ny elektrokatalysator til at omdanne kuldioxid til flydende brændstofKunstnerisk gengivelse af elektrokatalytisk proces til omdannelse af kuldioxid og vand til ethanol. Kredit:Kredit:Argonne National Laboratory Katalysatorer fremskynder kemiske reaktioner og danner
Forskere opdager ny elektrokatalysator til at omdanne kuldioxid til flydende brændstofKunstnerisk gengivelse af elektrokatalytisk proces til omdannelse af kuldioxid og vand til ethanol. Kredit:Kredit:Argonne National Laboratory Katalysatorer fremskynder kemiske reaktioner og danner -
 Rensning af luften:En reduktionsbaseret løsning på nitrogenforurening med en ny katalysatorEn ny jernkatalysator hjælper fortrinsvis med at reducere nitrogenoxid til hydroxylamin, åbne døre til forureningskontrol og ren energi. Kredit:Gwangju Institute of Science and Technology (GIST) V
Rensning af luften:En reduktionsbaseret løsning på nitrogenforurening med en ny katalysatorEn ny jernkatalysator hjælper fortrinsvis med at reducere nitrogenoxid til hydroxylamin, åbne døre til forureningskontrol og ren energi. Kredit:Gwangju Institute of Science and Technology (GIST) V -
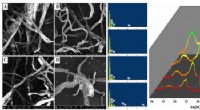 Forskere rapporterer effektiv brug af affaldspapir til cellulaseproduktion af Trichoderma longifloru…Figur 1. Strukturel karakterisering af affaldspapir. Til venstre:SEM (× 1000 forstørrelse) og EDS -analyse af affaldspapir (A, affald kontor papir; B, serviet; C, magasin papir; D, bølgepap); Til højr
Forskere rapporterer effektiv brug af affaldspapir til cellulaseproduktion af Trichoderma longifloru…Figur 1. Strukturel karakterisering af affaldspapir. Til venstre:SEM (× 1000 forstørrelse) og EDS -analyse af affaldspapir (A, affald kontor papir; B, serviet; C, magasin papir; D, bølgepap); Til højr -
 Det værdifulde bidrag fra stress til den termiske stabilitet af nanokornede polykrystallinske leger…Kredit:CC0 Public Domain Nanokornede metaller og legeringer, hvis kornstørrelse er mindre end 100 nm, udviser ekstrem høj styrke og høj duktilitet, har fremragende mekaniske egenskaber. Nanokorned
Det værdifulde bidrag fra stress til den termiske stabilitet af nanokornede polykrystallinske leger…Kredit:CC0 Public Domain Nanokornede metaller og legeringer, hvis kornstørrelse er mindre end 100 nm, udviser ekstrem høj styrke og høj duktilitet, har fremragende mekaniske egenskaber. Nanokorned
- Sådan bruger du en Bezel Slide Rule
- Sådan lyser du skærmen på et Texas Instruments TI-85 Calculator
- Hvor mange sanser har mennesker?
- Hvorfor HCl bruges til at opløse Ciprofloxacin pulver?
- Varm og generet:varme påvirker os alle, men ældre mennesker står over for de største sundhedsris…
- Meteor over Lake Michigan lyser himlen op i flere stater


