Hvordan forudsiger den anden lov om termodynamik adfærdsgasser?
1. Entropi og gasudvidelse:
* stigende entropi: Den anden lov siger, at entropien af et isoleret system altid øges over tid. I forbindelse med gasser betyder det, at gasser naturligt har en tendens til at udvide og besætte mere plads. Dette skyldes, at en mere udvidet tilstand har en højere entropi (mere mulige mikrostater eller måder, hvorpå gasmolekylerne kan arrangeres).
* spontan ekspansion: Hvis du frigiver en gas i en større beholder, vil den spontant udvide til at fylde hele volumenet. Dette skyldes, at ekspansionen øger systemets entropi.
2. Gasblandinger og entropi:
* blanding og entropi: Når to forskellige gasser blandes, øges systemets entropi. Dette skyldes, at der er flere måder at arrangere molekylerne af de forskellige gasser sammenlignet med at have dem adskilt.
* spontan blanding: Gasser blander spontant med hinanden på grund af stigningen i entropi. Dette forklarer, hvorfor for eksempel luft (en blanding af nitrogen, ilt og andre gasser) forbliver godt blandet.
3. Gastryk og entropi:
* tryk og entropi: Presset af en gas er relateret til den gennemsnitlige kinetiske energi af dens molekyler. Når en gas udvides, falder den gennemsnitlige kinetiske energi af dens molekyler, og trykket falder således. Dette fald i trykket er også knyttet til en stigning i entropi.
* ligevægt: Presset af en gas i en lukket beholder vil til sidst nå et punkt, hvor systemets entropi maksimeres. Dette er ligevægtstilstanden, hvor gassen er jævnt fordelt over beholderen.
4. Gasdiffusion og entropi:
* diffusion og entropi: Diffusion er processen, hvor gasser bevæger sig fra regioner med høj koncentration til regioner med lav koncentration. Denne proces er drevet af stigningen i entropi. Når gassen spreder sig, er der mere mulige arrangementer af molekylerne, hvilket fører til en højere entropi.
5. Temperatur og entropi:
* Temperatur og entropi: Entropien af en gas er direkte proportional med dens temperatur. Efterhånden som temperaturen på en gas øges, har molekylerne mere kinetisk energi og er mere tilbøjelige til at bevæge sig tilfældigt, hvilket øger entropien.
Kortfattet:
Den anden lov om termodynamik forklarer gennem begrebet entropi den spontane ekspansion, blanding, trykændringer, diffusion og temperaturafhængighed af gasser. Det giver en grundlæggende ramme for at forstå opførslen af disse væsentlige komponenter i vores verden.
Sidste artikelGiv en brug af termisk ekspansion i gasser?
Næste artikelEr Xenon en leder af elektrictiy?
 Varme artikler
Varme artikler
-
 Facil metode foreslået til mikrofabrikation på ikke-plane substraterFleksibel hulmaske muliggjorde mønsterdannelse af mikroskala hydrofil/hydrofob grænseflade på forskellige substrater. Kredit:YAN Shiqiang De fleste mikrofabrikationsteknologier er fokuseret på den
Facil metode foreslået til mikrofabrikation på ikke-plane substraterFleksibel hulmaske muliggjorde mønsterdannelse af mikroskala hydrofil/hydrofob grænseflade på forskellige substrater. Kredit:YAN Shiqiang De fleste mikrofabrikationsteknologier er fokuseret på den -
 En ny metode til installation af svovl i komplekse molekylerForskere, der arbejder i laboratoriet i Ben Shen, Ph.d., hos Scripps Research, Florida har fundet en ny familie af svovlinstallerende enzymer ved at udvinde bakteriernes genomer i deres samling af mik
En ny metode til installation af svovl i komplekse molekylerForskere, der arbejder i laboratoriet i Ben Shen, Ph.d., hos Scripps Research, Florida har fundet en ny familie af svovlinstallerende enzymer ved at udvinde bakteriernes genomer i deres samling af mik -
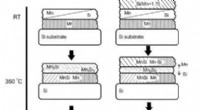 Fysikere overvåger dannelsen af film med højere mangansilicidSkematisk illustration af synteseproceduren til venstre:Mn17Si30 og højre Mn4Si7 -prøve. Kredit:Ivan Tarasov Et team fra Kirensky Institute of Physics (Siberian Branch of the Russian Academy of Sc
Fysikere overvåger dannelsen af film med højere mangansilicidSkematisk illustration af synteseproceduren til venstre:Mn17Si30 og højre Mn4Si7 -prøve. Kredit:Ivan Tarasov Et team fra Kirensky Institute of Physics (Siberian Branch of the Russian Academy of Sc -
 Teknik til at skabe medicin fri for bivirkningerJ. Julius Zhu sagde, at hovedideen bag forskningen var faktisk meget enkel, men det tog os mange år at få denne ting til at fungere. Kredit:Dan Addison, Universitetets kommunikation En ny teknik
Teknik til at skabe medicin fri for bivirkningerJ. Julius Zhu sagde, at hovedideen bag forskningen var faktisk meget enkel, men det tog os mange år at få denne ting til at fungere. Kredit:Dan Addison, Universitetets kommunikation En ny teknik
- Racisme på amtsniveau forbundet med øgede COVID-19-tilfælde og dødsfald
- Høst af ressourcer på Mars med plasmaer
- Ny opdagelse åbner for 3D-målinger af magnetisme
- Forskere finder en ny måde at producere chirale molekyler på, som kan bringe sikrere og mere overk…
- Om årstiderne i Marine Biome
- Hvilke beviser observerede du, der ville føre til at tro, at resten var kaliumchlorid?


