Hvilken erklæring understøttes af resultaterne af Rutherford og Gold Foil Experiment?
Her er hvorfor:
* eksperimentet: Rutherford fyrede alfa -partikler (positivt ladet) på et tyndt ark guldfolie.
* forventet resultat: Baseret på "blommepudding -modellen" af atomet, hvor positiv ladning blev antaget at være jævnt fordelt, skulle alfa -partiklerne være passeret med kun mindre afbøjninger.
* Faktisk resultat: De fleste alfa -partikler passerede lige igennem, men et lille antal blev afbøjet i store vinkler, og nogle sprang endda tilbage!
* Konklusion: Rutherford konkluderede, at den positive ladning for et atom skal koncentreres i en lille, tæt region, han kaldte kernen. De store afbøjninger og rebounds skyldtes alfa -partiklerne, der stødte på denne massive, positivt ladede kerne.
Eksperimentet gjorde ikke Støt ideen om, at atomer for det meste er tomt rum (selvom dette er en konsekvens af, at kernen er så lille). Det understøttede heller ikke "blomme budding -modellen", som blev modbevist af eksperimentet.
 Varme artikler
Varme artikler
-
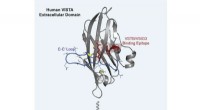 Ny indsigt i et kræftbeskyttende protein kan guide en ny generation af kræftbehandlingerVed hjælp af en kombination af beregning og eksperiment, forskere var i stand til at kortlægge formen på VISTA, et checkpoint protein, der forsvarer kræftceller mod immunsystemangreb, samt den del af
Ny indsigt i et kræftbeskyttende protein kan guide en ny generation af kræftbehandlingerVed hjælp af en kombination af beregning og eksperiment, forskere var i stand til at kortlægge formen på VISTA, et checkpoint protein, der forsvarer kræftceller mod immunsystemangreb, samt den del af -
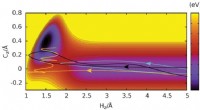 Forskere finder, at H-C-bindinger dannes, når brintatomer kolliderer med grafen med høj hastighedRehybridisering i dannelsen af en C-H-binding ved kollisioner af et H-atom på en grafenoverflade. HZ og CZ er afstandene mellem H- og C -atomerne fra grafenplanet. Tre baner er vist for H-atomer med
Forskere finder, at H-C-bindinger dannes, når brintatomer kolliderer med grafen med høj hastighedRehybridisering i dannelsen af en C-H-binding ved kollisioner af et H-atom på en grafenoverflade. HZ og CZ er afstandene mellem H- og C -atomerne fra grafenplanet. Tre baner er vist for H-atomer med -
 En kold opblødning sænker risikoen for salmonellavækst på spirede fødevarerKorn, frø og nødder, der er lagt i blød i koldt vand. Kredit:Joy Waite-Cusic, Oregon State University Iblødsætning af spirede fødevarer i koldt vand, snarere end den mere almindelige praksis med i
En kold opblødning sænker risikoen for salmonellavækst på spirede fødevarerKorn, frø og nødder, der er lagt i blød i koldt vand. Kredit:Joy Waite-Cusic, Oregon State University Iblødsætning af spirede fødevarer i koldt vand, snarere end den mere almindelige praksis med i -
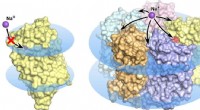 Biofysikere løser den sande struktur af meget lovende optogenetisk protein KR2 rhodopsinKR2 rhodopsin monomer (venstre) og pentamer (højre) i cellemembranen, vist som blå diske. I monomer tilstand, natriumtransport er blokeret, den orange pore tillader ikke ionoptagelse i proteinet. Kred
Biofysikere løser den sande struktur af meget lovende optogenetisk protein KR2 rhodopsinKR2 rhodopsin monomer (venstre) og pentamer (højre) i cellemembranen, vist som blå diske. I monomer tilstand, natriumtransport er blokeret, den orange pore tillader ikke ionoptagelse i proteinet. Kred
- Hvordan kan menneskeskabte klimaændringer bevises?
- Hvilken del af procesvidenskaben passer til kontinenter, der matcher fossiler på forskellige og lig…
- En kraftfuld ny teknik gør det muligt for forskere at studere, hvordan proteiner ændrer form inde …
- Skovbrande bringer klimaets mørke kræfter til stratosfæren
- Hvilke komponenter i plasmamembranen en dyrecelle ville du finde på sin inderste overflade direkte …
- Hvad er tilpasningerne af et kokosfrø?


