Hvordan forklarede John Dalton en kemisk reaktion ved hjælp af sin atomteori?
1. Atomer er de grundlæggende byggesten: Dalton foreslog, at alle stof er sammensat af udelelige partikler kaldet atomer. Dette betød, at kemiske reaktioner involverer omarrangement af disse atomer, ikke deres skabelse eller ødelæggelse.
2. Atomer af et element er identiske: Dalton mente, at alle atomer i et specifikt element er identiske i masse og egenskaber. Dette betød, at forholdet mellem atomer i en kemisk reaktion ville blive fastlagt, hvilket førte til loven i bestemte proportioner.
3. Atomer kombineres i hele talforhold: Dalton foreslog, at atomer af forskellige elementer kombineres i enkle forhold mellem hele antal for at danne forbindelser. Dette forklarede loven i flere proportioner, hvor forskellige forbindelser fremstillet af de samme elementer har forskellige forhold mellem disse elementer.
4. Atomer oprettes hverken eller ødelægges i kemiske reaktioner: Daltons teori antydede, at kemiske reaktioner involverer adskillelse, kombination eller omarrangement af atomer. Det samlede antal atomer af hver type forbliver konstant.
Daltons forklaring af en kemisk reaktion:
Lad os tage det enkle eksempel på reaktionen mellem brint og ilt for at danne vand:
* før reaktionen: Brint findes som diatomiske molekyler (H 2 ) og ilt findes som diatomiske molekyler (O 2 ).
* Under reaktionen: Brint- og iltmolekylerne går i stykker og frigiver individuelle brint- og iltatomer. Disse atomer rekombineres derefter i et nyt arrangement, der danner vandmolekyler (H 2 O).
* efter reaktionen: Antallet af brint- og iltatomer forbliver det samme, men de er nu organiseret i vandmolekyler.
Sammenfattende, ifølge Daltons atomteori:
* Kemiske reaktioner involverer omarrangement af atomer, ikke deres skabelse eller ødelæggelse.
* Forholdet mellem atomer i en reaktion er fast, hvilket resulterer i bestemte proportioner.
* Atomer kombineres i forhold mellem hele antal for at danne forbindelser.
Disse principper gav en klar og forståelig ramme for forståelse af kemiske reaktioner, der lå grundlaget for fremtidige fremskridt inden for kemi.
 Varme artikler
Varme artikler
-
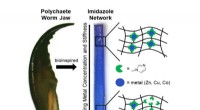 Forskere efterligner en ormedødelig kæbe for at designe og danne elastiske materialerForskere skabte en bioinspireret gradient i mekaniske egenskaber. Området opnås ved at programmere tætheden af en speciel interaktion mellem metalioner og elektrondonerende ligander. Det venstre bil
Forskere efterligner en ormedødelig kæbe for at designe og danne elastiske materialerForskere skabte en bioinspireret gradient i mekaniske egenskaber. Området opnås ved at programmere tætheden af en speciel interaktion mellem metalioner og elektrondonerende ligander. Det venstre bil -
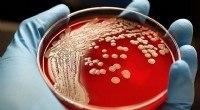 Forskere udvikler en ny forbindelse, som dræber begge typer antibiotika-resistente superbugsKredit:University of Sheffield Forskere ved University of Sheffield har udviklet en ny forbindelse, der er i stand til at dræbe både gram-positive og gram-negative antibiotikaresistente bakterier.
Forskere udvikler en ny forbindelse, som dræber begge typer antibiotika-resistente superbugsKredit:University of Sheffield Forskere ved University of Sheffield har udviklet en ny forbindelse, der er i stand til at dræbe både gram-positive og gram-negative antibiotikaresistente bakterier. -
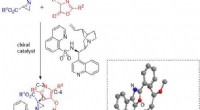 Asymmetrisk syntese af aziridin med en ny katalysator kan hjælpe med at udvikle nye lægemidlerFremstilling af aziridiner med højt udbytte og høj renhed ved hjælp af ny katalysator. Forskere fra Japan foreslog for nylig en mulig overgangstilstand for reaktionen mellem aziridiner og oxazoloner i
Asymmetrisk syntese af aziridin med en ny katalysator kan hjælpe med at udvikle nye lægemidlerFremstilling af aziridiner med højt udbytte og høj renhed ved hjælp af ny katalysator. Forskere fra Japan foreslog for nylig en mulig overgangstilstand for reaktionen mellem aziridiner og oxazoloner i -
 Nøglebyggesten til organiske molekyler opdaget i meteoritterEt fragment af Murchison-meteoritten, en af de tre kulstofrige meteoritter, der blev udtaget i denne undersøgelse. Kredit:Daniel P. Glavin Forskere fra Japan og USA har bekræftet tilstedeværelse
Nøglebyggesten til organiske molekyler opdaget i meteoritterEt fragment af Murchison-meteoritten, en af de tre kulstofrige meteoritter, der blev udtaget i denne undersøgelse. Kredit:Daniel P. Glavin Forskere fra Japan og USA har bekræftet tilstedeværelse


