Hvordan forholder elektriske ladninger sig til dele af et atom?
1. Atomets struktur:
* Protoner: Beliggende i atomets kerne (center). De bærer en positiv (+) opladning .
* neutroner: Også placeret i kernen. De bærer uden gebyr (de er neutrale).
* Elektroner: Bane kernen i skaller eller energiniveau. De bærer en negativ (-) opladning .
2. Opladningsbalance og neutralitet:
* I et neutralt atom svarer antallet af protoner (positive ladninger) på antallet af elektroner (negative ladninger). Dette skaber en afbalanceret tilstand, hvilket betyder, at atomet ikke har nogen nettoafgift.
3. Ioner:
* Når et atom vinder eller mister elektroner, bliver det en ion.
* kationer: Atomer, der mister elektroner, bliver positivt ladede.
* anioner: Atomer, der får elektroner, bliver negativt ladet.
4. Kemisk binding:
* Tiltrækningen mellem modsatte afgifter (protoner og elektroner) spiller en afgørende rolle i kemisk binding.
* Atomer kan dele elektroner (kovalent binding) eller overføre elektroner (ionisk binding) til dannelse af molekyler og forbindelser.
5. Elektrisk strøm:
* Strømmen af elektrisk strøm er i det væsentlige bevægelse af elektroner.
* I ledere kan elektroner bevæge sig frit, hvilket giver mulighed for strøm af elektricitet.
* I isolatorer er elektroner tæt bundet, hvilket gør dem til dårlige ledere.
Kortfattet:
De elektriske egenskaber af atomer bestemmes primært af tilstedeværelsen af protoner (positive) og elektroner (negativ). Arrangementet og interaktionen af disse ladede partikler påvirker, hvordan atomer interagerer med hinanden og danner alt omkring os.
Sidste artikelEn ideel gas er en der?
Næste artikelHvilken er en erklæring om den anden lovtermodynamik?
 Varme artikler
Varme artikler
-
 Opskalering af biohybride systemer til syntetisering af brændstoffer, kemikalierVisualisering af en bakteriecelle (øverst), der omdanner organiske molekylers kemiske energi til elektroner, der overføres til en uorganisk tinoxidkatalysator (nederst) via molekylære ledninger indlej
Opskalering af biohybride systemer til syntetisering af brændstoffer, kemikalierVisualisering af en bakteriecelle (øverst), der omdanner organiske molekylers kemiske energi til elektroner, der overføres til en uorganisk tinoxidkatalysator (nederst) via molekylære ledninger indlej -
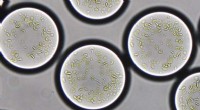 Forskere udvikler en kunstig kloroplastPlantethylacoider er indkapslet i mikrodråber på cirka 90 mikrometer i diameter. Udstyret med et sæt enzymer, de semisyntetiske kloroplaster fikserer kuldioxid ved hjælp af solenergi, efter naturens e
Forskere udvikler en kunstig kloroplastPlantethylacoider er indkapslet i mikrodråber på cirka 90 mikrometer i diameter. Udstyret med et sæt enzymer, de semisyntetiske kloroplaster fikserer kuldioxid ved hjælp af solenergi, efter naturens e -
 Søger havet, og bakteriekampe, til nye antibiotikaCameron Currie, ret, med den amerikanske energiminister Steven Chu i Microbial Sciences Building i 2012. Kredit:Jeff Miller Alexander Flemings opdagelse af penicillin - verdens første naturlige an
Søger havet, og bakteriekampe, til nye antibiotikaCameron Currie, ret, med den amerikanske energiminister Steven Chu i Microbial Sciences Building i 2012. Kredit:Jeff Miller Alexander Flemings opdagelse af penicillin - verdens første naturlige an -
 Celleadfærd, engang indhyllet i mystik, afsløres i nyt lysGavin King og et team af forskere ved University of Missouri er et skridt tættere på at forstå celleadfærd ved hjælp af et specialiseret mikroskop. Kredit:University of Missouri-Columbia En celles
Celleadfærd, engang indhyllet i mystik, afsløres i nyt lysGavin King og et team af forskere ved University of Missouri er et skridt tættere på at forstå celleadfærd ved hjælp af et specialiseret mikroskop. Kredit:University of Missouri-Columbia En celles


